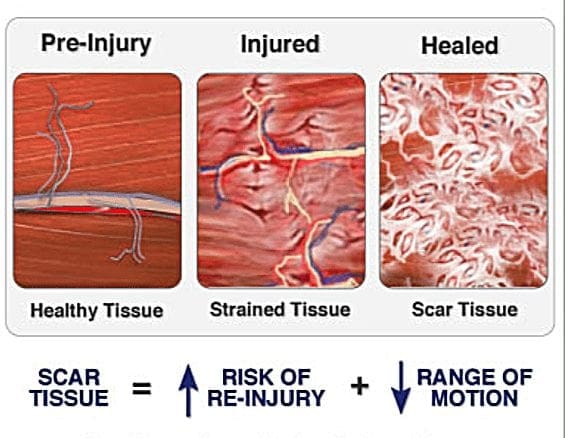
Механизми пута модулације бола у Ел Пасу, Тексас
Већина, ако не и све, болести тела изазивају бол. Бол се тумачи и осећа у мозгу. Бол се модулира помоћу две кључне врсте лекова који делују на мозак: аналгетици и анестетици. Термин аналгетик се односи на лек који ублажава бол без губитка свести. Израз централна анестезија односи се на лек који депресира ЦНС. Одликује се недостатком сваке перцепције чулних модалитета, на пример, губитак свести без губитка критичних функција.
опијатна аналгезија (ОА)
Најуспешнији клинички коришћени лекови за производњу привремене аналгезије и ублажавање бола су опиоидни лекови, који укључују морфијум и хероин. Тренутно не постоје додатне моћне терапијске опције против опијата. Неколико нежељених ефеката узрокованих употребом опијата укључује толеранцију и зависност од дрога или зависност. Генерално, ови лекови модулишу долазне информације о болу у кичми и централном нервном систему, поред тога што привремено ублажавају бол, а могу се назвати и аналгезија која производи опијате (ОА). Антагонист опијата је лек који антагонизује опиоидне ефекте, као што су налоксон или малтроксон, итд. Они су компетитивни антагонисти опијатних рецептора. Међутим, мозак има неуронско коло и ендогене супстанце које модулирају бол.
Ендогени опиоиди
Опиоидергична неуротрансмисија се налази у целом мозгу и кичменој мождини и верује се да утиче на многе функције централног нервног система или ЦНС-а, као што су ноцицепција, кардиоваскуларне функције, терморегулација, дисање, неуроендокрине функције, неуроимуне функције, потрошња хране, сексуална активност, конкурентност. локомоторно понашање као и памћење и учење. Опиоиди имају изражене ефекте на расположење и мотивацију и изазивају осећај еуфорије.
Идентификоване су три класе опиоидних рецептора: ?-му, ?-делта и ?-капа. Све 3 класе су широко распрострањене у мозгу. Гени који кодирају сваки од њих су клонирани и утврђено је да функционишу као чланови рецептора Г протеина. Штавише, три главна типа ендогених опиоидних пептида који ступају у интеракцију са горе наведеним опијатним рецепторима су препозната у централном нервном систему, укључујући ?-ендорфине, енкефалине и динорфине. Ова 3 опиоидна пептида потичу из великог протеинског рецептора помоћу три различита гена, као што су ген за проопиомеланокортин или ПОМЦ, ген за проенкефалин и ген за продинорфин. Опиоидни пептиди модулирају ноцицептивни унос на два начина: прво, блокирају неуротрансмитер ослобађају се инхибирањем прилива Ца2+ у пресинаптички терминал, или друго, отварају калијумове канале, што хиперполаризује неуроне и инхибира шик активност. Делују на различите рецепторе у мозгу и кичменој мождини.
Енкефалини се сматрају претпостављеним лигандима за ? рецептори, ? ендорфине за своје ?-рецепторе, и динорфине за ? рецептори. Различити типови опиоидних рецептора су различито распоређени унутар периферног и централног нервног система, или ЦНС. Постоје докази о функционалним разликама у овим рецепторима у различитим структурама. Ово објашњава зашто се многи нежељени нежељени ефекти јављају након третмана опијатима. На пример, ми (?) рецептори су широко распрострањени у парабрахијалним језгрима можданог стабла, где респираторни центар и инхибиција ових неурона могу изазвати оно што је познато као респираторна депресија.
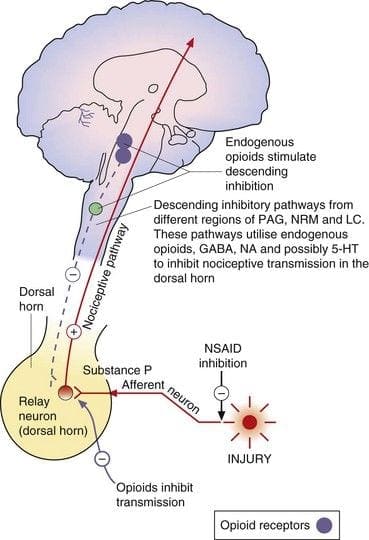
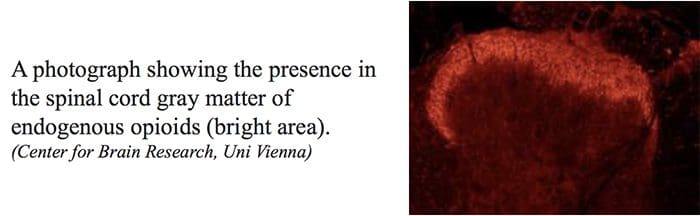
Централни или периферни терминали ноцицептивних аферентних влакана имају опијатне рецепторе у којима егзогени и ендогени опиоиди могу да делују тако да модулишу способност преношења ноцицептивних информација. Поред тога, висока густина опијатних рецептора налази се у периакведукталном сивом, или ПАГ, нуцлеус рапхе магнус, или НРМ, и дорзалном рапхе, или ДР, из ростралне вентралне мождине, у кичменој мождини, каудатном језгру или ЦН, септалном језгру, хипоталамус, хабенула и хипокампус.�Системски примењени опиоиди у дозама аналгетика активирају кичмене и супраспиналне механизме преко ?, ? и ? укуцавају опиоидне рецепторе и регулишу сигнале бола како би модулирали симптоме.
Неуронска кола и модулација бола
Дуги низ деценија сугерисало се да негде у централном нервном систему постоји коло које може модулирати долазне детаље бола. Теорија контроле капије и систем за пренос бола узлазно/силазни су два предлога таквог кола. У наставку ћемо детаљније разговарати о оба.
Теорија контроле капије
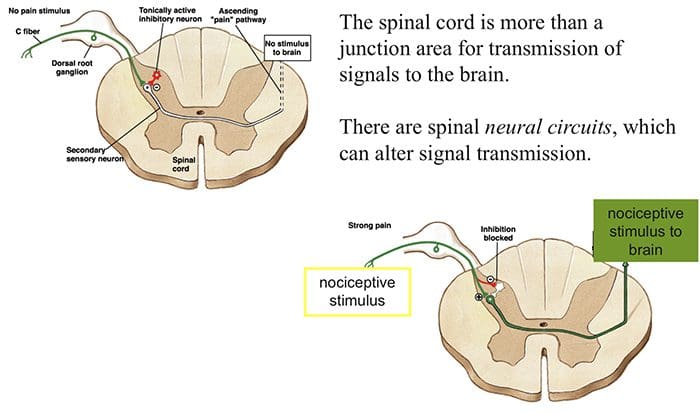
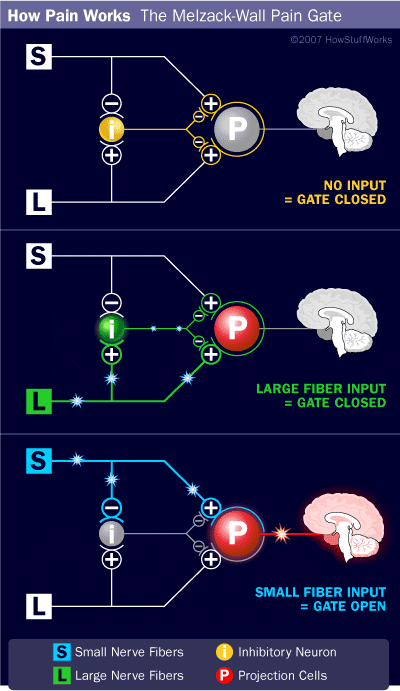
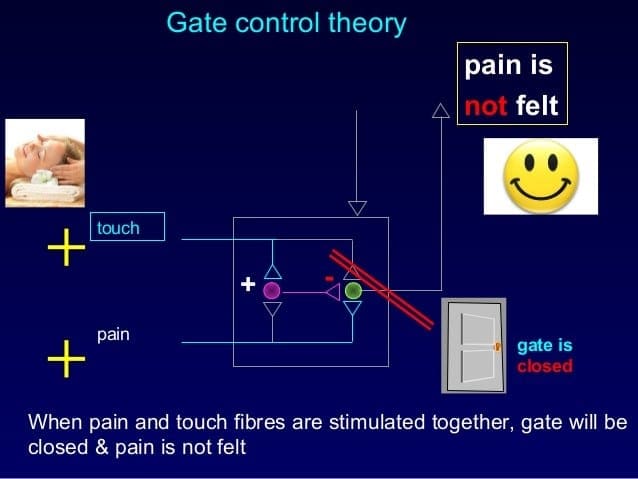
Почетни механизам модулације бола познат као теорија контроле капије, предложили су Мелзак и Вол средином 1960-их. Појам теорије контроле капије је да не-болни унос затвара капије болном улазу, што резултира избегавањем сензације бола од путовања у ЦНС, на пример, нешкодљив унос или стимулација потискује бол.
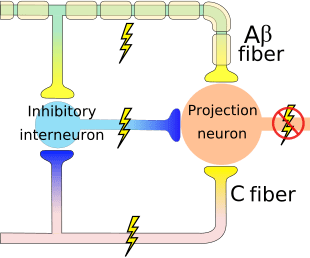
Теорија имплицира да колатерали великих сензорних влакана који носе кожни сензорни улаз активирају инхибиторне интернеуроне, који инхибирају и регулишу пренос података о болу који се преносе из влакана бола. Унос који није штетан инхибира бол, или сензорни унос, и затвара капију за штетни унос. Теорија контроле капије показује да ће на нивоу кичмене мождине, нешкодљива стимулација створити пресинаптичку инхибицију на влакнима ноцицептора дорзалног корена која синапсе на спиналним неуронима ноцицептора (Т). Ова пресинаптичка инхибиција ће такође спречити долазне штетне информације да стигну у ЦНС, на пример, затвориће капију долазних токсичних информација.
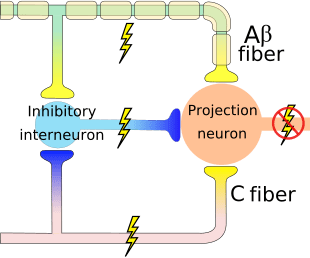
Теорија контроле капије била је образложење за идеју производње и употребе транскутане електричне нервне стимулације, или ТЕНС, за ублажавање болова. Да би била ефикасна, ТЕНС јединица генерише две различите присутне фреквенције испод прага бола који пацијент може да примени. Овај процес је показао одређени степен достигнућа у лечењу хроничног бола.
Модулација бола: теорија контроле капије
Аналгезија изазвана стимулацијом (СПА)
Доказ за инхерентни систем аналгезије пронађен је интракранијалном електричном стимулацијом одређених дискретних региона мозга. Ове области би биле периакведуктално сиво, или ПАГ, и нуцлеус рапхе магнус, или НРМ, дорзално рапхе, или ДР, каудатно језгро, или ЦН, септално језгро, или Спт, заједно са другим језгрима. Таква стимулација или сензорни сигнали, инхибирају бол, чинећи аналгезију без супресије понашања, док осећај додира, температуре и притиска остаје нетакнут. Према истраживачким студијама, СПА, или аналгезија изазвана стимулацијом, је израженија и траје дужи временски период након стимулације код људи него код експерименталних животиња. Поред тога, током СПА, субјекти, међутим, и даље реагују на безболну стимулацију као што су температура и додир унутар ограниченог региона аналгезије. Најефикаснији ЦНС, или региони централног нервног система за СПА, били би у ПАГ и језгри рапхе, или РН.
Електрична стимулација ПАГ-а или НРМ-а инхибира ћелије таламуса кичме или кичмене неуроне који се пројектују моносинаптички на таламус, у ламинама И, ИИ и В да би се обезбедиле штетне информације од ноцицептора који су на крају модулисани на нивоу кичмене мождине. Штавише, ПАГ има неуронске везе са нуцлеус рапхе магнус, или НРМ.
Активност ПАГ-а се највероватније јавља активацијом силазног пута из НРМ-а, а вероватно и активацијом узлазних веза које делују на веће субкортикалне нивое ЦНС-а. Поред тога, електрична стимулација ПАГ-а или НРМ-а производи бихевиоралну аналгезију или аналгезију изазвану стимулацијом. Стимулација производи аналгезију или СПА изазива ослобађање ендорфина који може бити блокиран опијатним антагонистом налоксоном.
Током ПАГ и/или РН стимулације, серотонин, који се у медицини такође назива 5-ХТ, такође може да се отпусти из узлазних и силазних аксона из субкортикалних језгара, у језгри кичменог тригеминуса и кичмене мождине. Ово ослобађање 5-ХТ модулира и регулише пренос бола инхибирањем или блокирањем долазног неуронског деловања. Смањење 5-ХТ електричном лезијом рапхе језгара или неуротоксичном лезијом изазваном локалном ињекцијом хемијског агенса као што је парахлорофенилаланин, или ПЦПА, доводи до блокирања моћи опијата, како интракранијалног тако и системског, као и снаге опијата. електрична стимулација како би се произвела аналгезија.
Да би се потврдило да ли је електрична стимулација изазвала аналгезију путем ослобађања опијата и допамина, тада се у регион локално микроињектује морфијум или 5-ХТ. Све ове микроињекције на крају стварају аналгезију. Ови процеси такође обезбеђују начин да се идентификују области мозга које се односе на сузбијање бола и помажу да се направи мапа центара за бол. Најефикаснији начин за производњу опијатне аналгезије, или ОА, је интрацеребрална ињекција морфијума у ПАГ.
ПАГ и РН, као и друге мождане структуре у којима се производи аналгезија, такође су богати опијатним рецепторима. Интрацеребрална примена опиоида довела је до аналгезије и СПА се може блокирати системским или локалним микроињекцијама налоксона, антагониста морфијума, у ПАГ или РН. Из тог разлога, сугерисано је да ова два, и ОА и СПА, делују честим механизмом.
Ако се ОА и СПА понашају кроз исти унутрашњи систем, онда је хипотеза да опијати активирају механизам за сузбијање бола много вероватнија. У ствари, тренутни докази сугеришу да микроињекције опијата у ПАГ активирају еферентни систем можданог стабла који инхибира пренос бола на сегментним нивоима кичмене мождине. Ова запажања имплицирају да аналгезија изазвана периакведукталном сивом, или ПАГ, захтева силазни пут у кичмену мождину.

Увид др Алек Јименез-а
Модулација бола настаје кроз процес електричне стимулације мозга који настаје услед активације силазних инхибиторних влакана, која регулишу или инхибирају улаз и излаз одређених неурона. Оно што је описано као опиоидни и серотонергички антагонисти, верује се да преокреће и локалну опијатну аналгезију и аналгезију изазвану можданим стимулансима. Сензорне сигнале или импулсе у централном нервном систему на крају контролишу и узлазни и силазни инхибиторни системи, користећи ендогене опиоиде или друге ендогене супстанце, као што је серотонин као инхибиторне медијаторе. Бол је сложена перцепција на коју такође могу утицати низ других фактора, укључујући емоционално стање.
Механизми модулације бола
Узлазни и силазни механизам за сузбијање бола
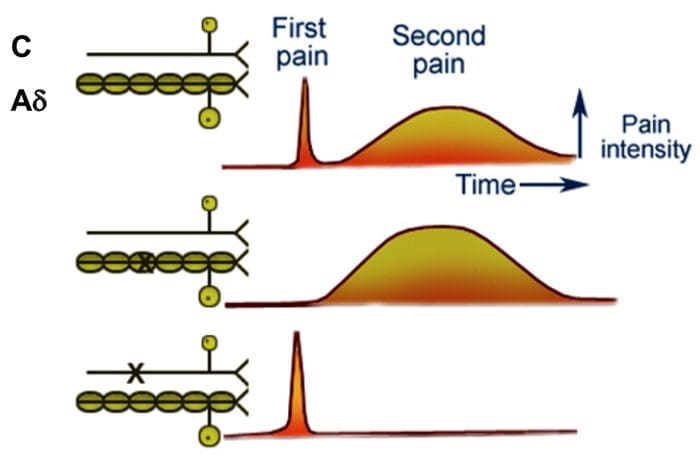
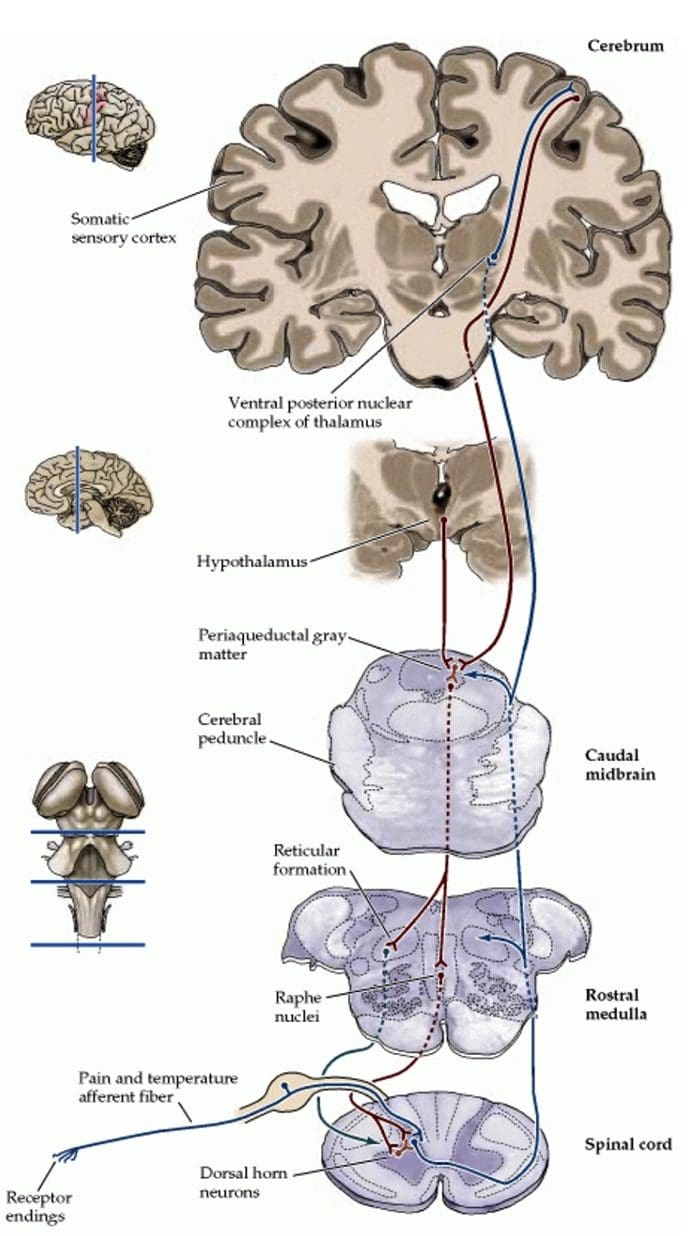
Примарна узлазна влакна бола, као што је А? и Ц влакна, долазе до дорзалног рога кичмене мождине из периферних нервних подручја како би инервирали ноцицепторске неуроне у Рекед ламинама И и ИИ. Ћелије из Рекед ламине ИИ праве синаптичке везе у Рекед слојевима ИВ до ВИИ. Ћелије, посебно унутар ламина И и ВИИ дорзалног рога, доводе до узлазних спиноталамичких тракта. На нивоу кичме, опијатни рецептори се налазе у пресинаптичким завршецима њихових ноцинеурона и у слојевима интернеуралног нивоа ИВ до ВИИ од дорзалног рога.
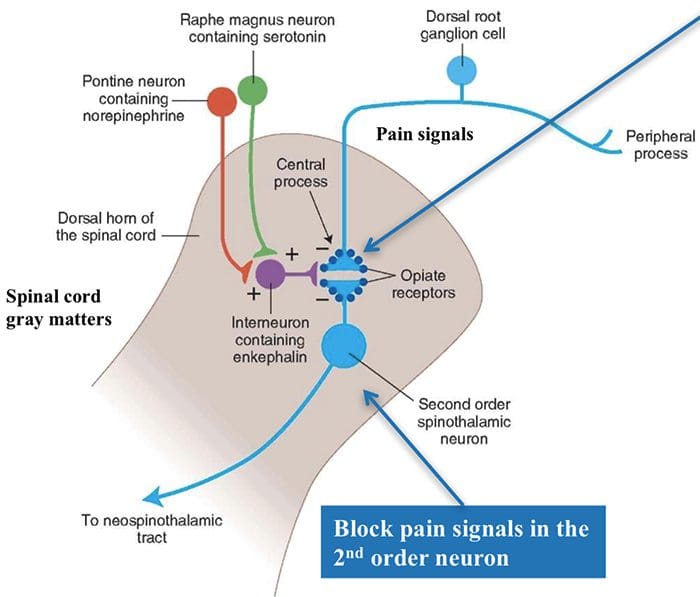
Активација опијатних рецептора на интернеуронском нивоу доводи до хиперполаризације неурона, што доводи до инхибиције активације као и ослобађања супстанце П, неуротрансмитера укљученог у пренос бола, чиме се спречава преношење бола. Круг који се састоји од периакведукталне сиве, или ПАГ, материје у горњем можданом стаблу, лоцус цоерулеус, или ЛЦ, нуцлеус рапхе магнус, или НРМ, и нуцлеус ретицуларис гигантоцеллуларис, или Ргц, доводи до опадајућег бола пут потискивања, који инхибира долазне податке о болу на нивоу кичмене мождине.
Као што је раније речено, опиоиди ступају у интеракцију са опијатним рецепторима на различитим нивоима централног нервног система. Ови опијатни рецептори су нормални циљни региони за хормоне и ендогене опијате, као што су ендорфини и енкефалини. Због везивања на рецептору у субкортикалним веб локацијама, секундарне промене које резултирају неким променама у електрофизиолошким особинама неурона и регулацији њихове информације о растућем болу.
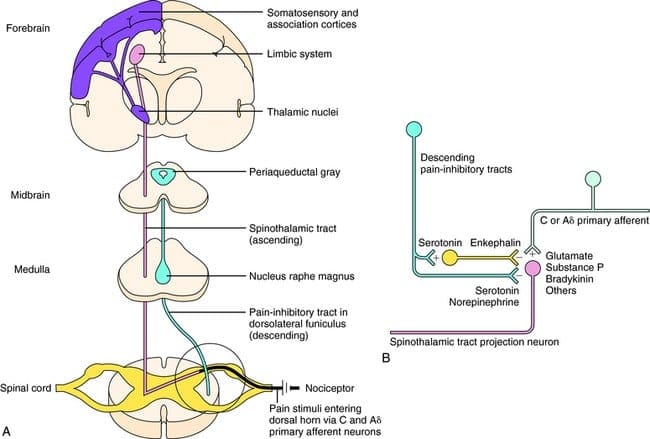
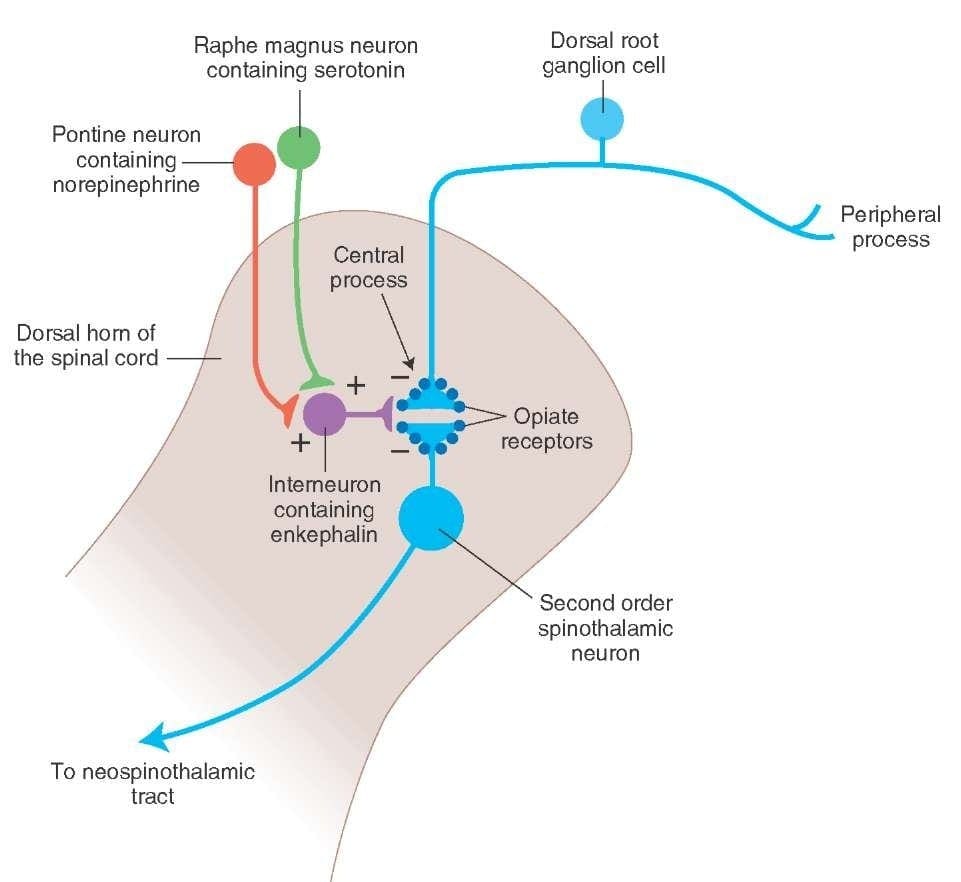
Шта активира ПАГ да изврши своје последице? Откривено је да штетна стимулација покреће неуроне у нуцлеус ретицуларис гигантоцеллуларис, или РГЦ. Језгро Ргц инервира и ПАГ и НРМ. ПАГ шаље аксоне у НРМ, а нерви у НРМ шаљу своје аксоне у кичмену мождину. Поред тога, билатералне лезије дорсолатералног фуницулуса, или ДЛФ, које се називају ДЛФКС, блокирају аналгезију произведену и електричном стимулацијом и микроињектирањем опијата директно у ПАГ и НРМ, али оне само умањују системске аналгетичке ефекте опијата. Ова запажања подржавају хипотезу да су дискретни силазни путеви из ДЛФ-а неопходни и за ОА и за СПА.
ДЛФ се састоји од влакана која потичу из неколико језгара можданог стабла, која могу бити серотонергична, или 5-ХТ, од нерава који се налазе унутар нуцлеус рапхе магнус, или НРМ; допаминергички неурони који потичу из вентралног тегменталног подручја, или ВТА, и адренергички неурони који потичу из лоцус цоерулеуса, или ЛЦ. Ова силазна влакна потискују штетни унос у ноцицептивне неуроне кичмене мождине у ламинама И, ИИ и В.
Опијатни рецептори су такође откривени у дорзалном рогу кичмене мождине, углавном у Рекед ламинама И, ИИ и В, и такви спинални опијатни рецептори посредују у инхибиторним ефектима на неуроне дорзалног рога који преносе ноцицептивне информације. Чини се да се дејство морфијума подједнако врши на језгра кичмене мождине и можданог стабла, укључујући ПАГ и НРМ. Системски морфијум делује на опијатне рецепторе можданог стабла и кичмене мождине како би произвео аналгезију. Морфијум везује опијатске рецепторе можданог стабла, што покреће силазни серотонергички пут можданог стабла у кичмену мождину, као и ДЛФ, а они имају синапсу посредовану опиоидима на нивоу кичмене мождине.
Ово запажање показује да штетни стимуланси, уместо нештетних стимулуса, одређују теорију контроле капије, која је критична за активацију силазног кола модулације бола где бол инхибира бол путем силазног ДЛФ пута. Поред тога, постоје узлазне везе у ПАГ и рапхе језгри у ПФ-ЦМ комплекс. Ови таламички региони су део модулације узлазног бола на степену диенцефалона.
Аналгезија изазвана стресом (СИА)
У одређеним стресним околностима може доћи до аналгезије. Изложеност многим различитим стресним или болним догађајима ствара аналгетички одговор. Овај феномен је познат као аналгезија изазвана стресом или СИА. Верује се да аналгезија изазвана стресом даје увид у физиолошке и психолошке факторе који покрећу ендогену контролу бола и системе опијата. На пример, војници повређени у битци или спортисти повређени у спорту понекад кажу да не осећају бол или нелагодност током битке или утакмице, али ће проћи кроз бол након тога када специфична ситуација престане. Код животиња је показано да електрични удари изазивају стрес изазвану аналгезију. На основу ових експеримената, претпоставља се да је притисак који су војници и спортисти искусили потиснуо бол који ће касније искусити.
Верује се да се ендогени опијати производе као одговор на стрес и инхибирају бол тако што покрећу силазни систем средњег мозга. Штавише, неке СИА су показале унакрсну толеранцију са опијатном аналгезијом, што указује да је ова СИА посредована преко опијатних рецептора. Експерименти који користе различите параметре стимулације електричним шоком показују такву аналгезију изазвану стресом и неке од оних анксиозности које производе аналгезију могу бити блокиране опиоидним антагонистом налоксоном, док друге нису блокиране налоксоном. У закључку, ова запажања доводе до одлуке да постоје и опијатски и неопијатни облици СИА.
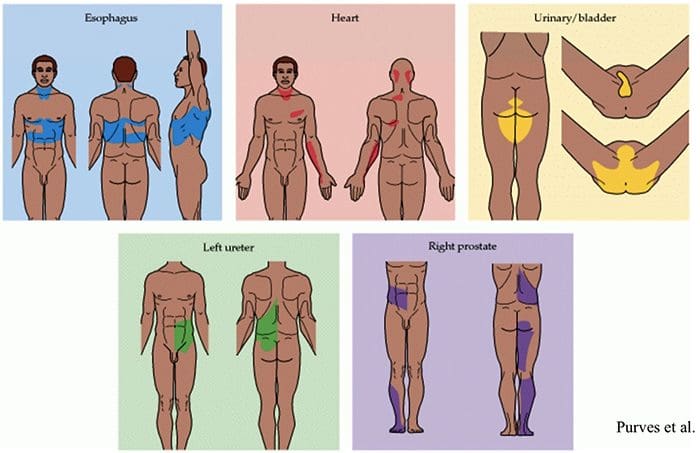
Соматовисцерални рефлекс
Соматовисцерални рефлекс је рефлекс у коме се висцералне функције активирају или инхибирају соматском сензорном стимулацијом. Код експерименталних животиња доказано је да и штетна и нешкодљива стимулација соматских аферената изазивају рефлексне промене у симпатичкој еферентној активности и, последично, функцији ефекторских органа. Ове појаве су се показале у регионима као што су гастроинтестинални тракт, уринарни тракт, мождина надбубрежне жлезде, лимфне ћелије, срце и судови мозга и периферни нерви.
Најчешће се инцизије добијају експериментално стимулацијом кожних аферената, иако су неки радови обављени и на мишићним и зглобним аферентима, укључујући ћелије кичменог стуба. Крајњи одговори ће представљати интеграцију вишеструких тоничних и рефлексних утицаја и могу показати латералне и сегментне трендове, као и променљиву ексцитабилност у складу са укљученим аферентима. С обзиром на сложеност и вишеструкост механизама укључених у последњу експресију рефлексног одговора, покушаји екстраполације на клиничке ситуације би највероватније требало да буду спроведени у корист даљих систематских физиолошких студија.
Опсег наших информација ограничен је на киропрактику, као и на повреде и стања кичме. Да бисте разговарали о теми, слободно питајте доктора Јименеза или нас контактирајте на 915-850-0900 .
Курирао др Алек Јименез
Додатне теме: ишијас
ишијас медицински се назива скупом симптома, а не појединачном повредом и / или стањем. Симптоми болова ишијасног нерва или ишијаса могу се разликовати у учесталости и интензитету, међутим, најчешће се описују као изненадни, оштри (налик ножу) или електрични болови који зраче из доњег дела леђа низ задњицу, кукове, бутине и ноге у стопало. Остали симптоми ишијаса могу укључивати пецкање или пецкање, утрнулост и слабост дуж дужине ишијасног нерва. Ишијас најчешће погађа особе старости између 30 и 50 година. Често се може развити као резултат дегенерације кичме због старости, међутим, компресија и иритација ишијасног нерва изазвана испупчењем или херниатед дисц, међу осталим здравственим проблемима кичме, такође може изазвати бол ишијалног нерва.

ЕКСТРА ВАЖНА ТЕМА: Симптоми ишијаса код киропрактичара



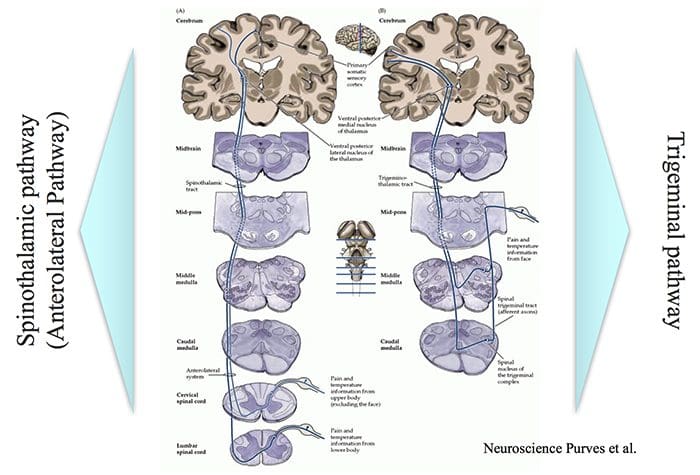
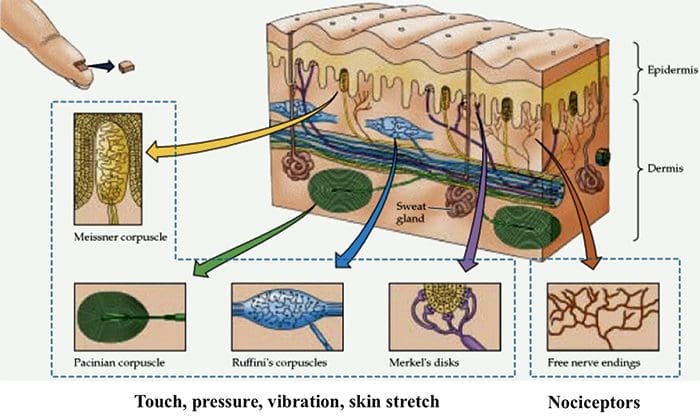
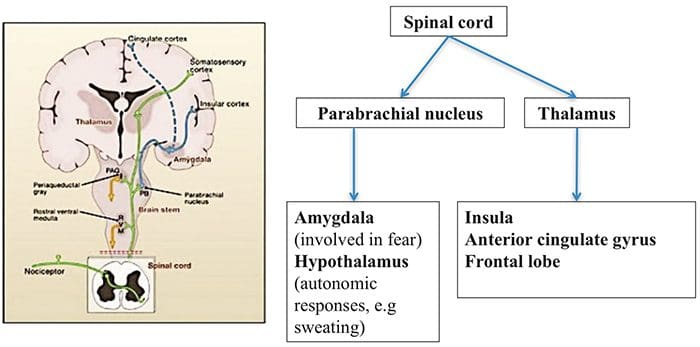 Подручја мозга укључена у обраду ноцицептивних сигнала
Подручја мозга укључена у обраду ноцицептивних сигнала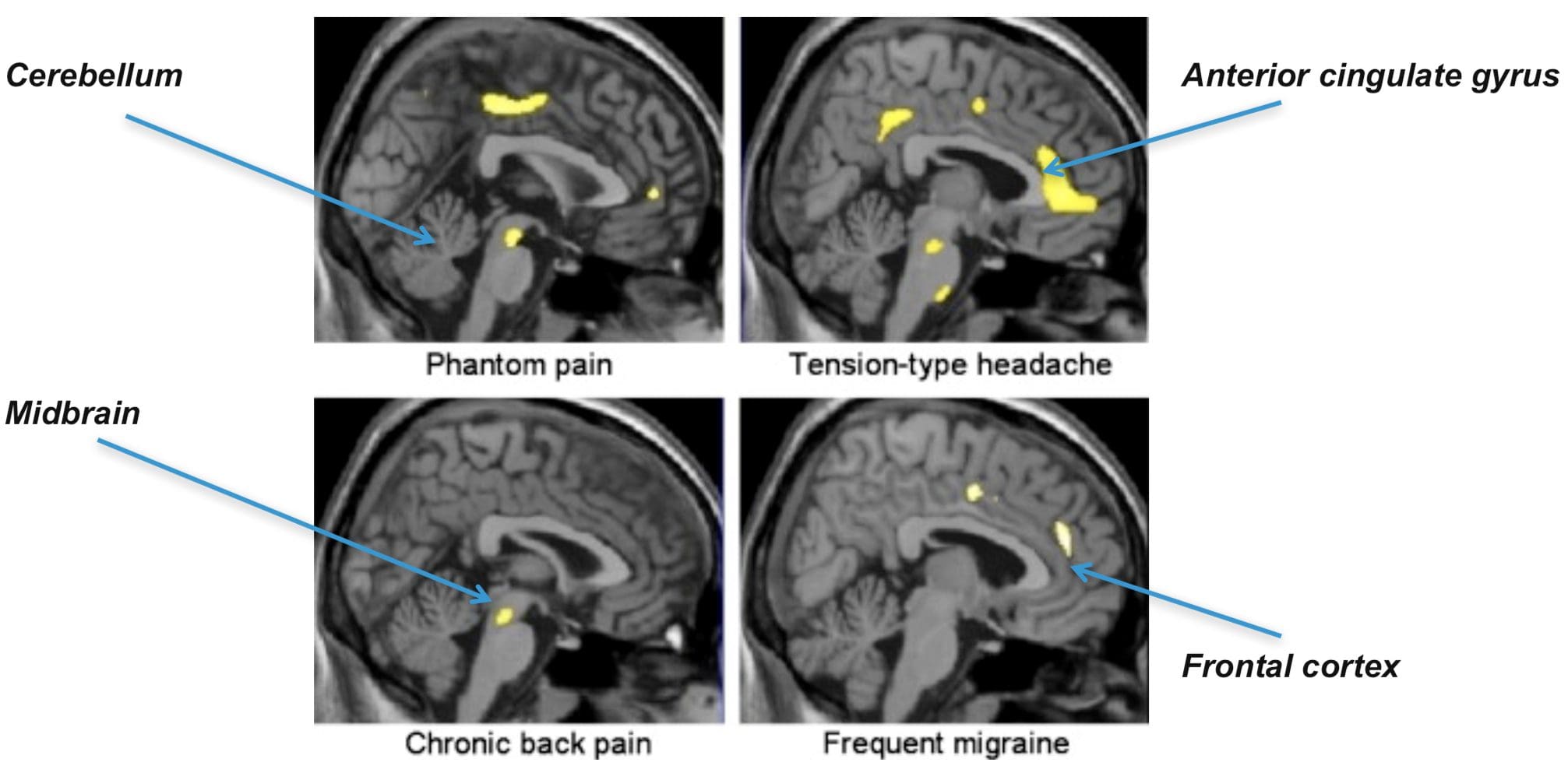 Предњи сингулат и кортекс инсула су активирани код људи
Предњи сингулат и кортекс инсула су активирани код људи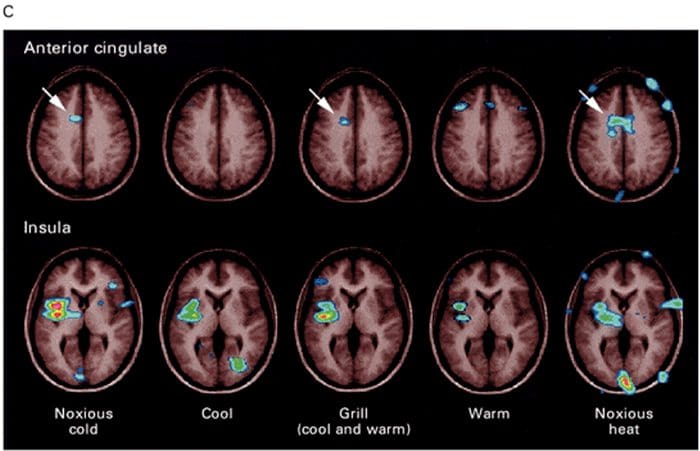
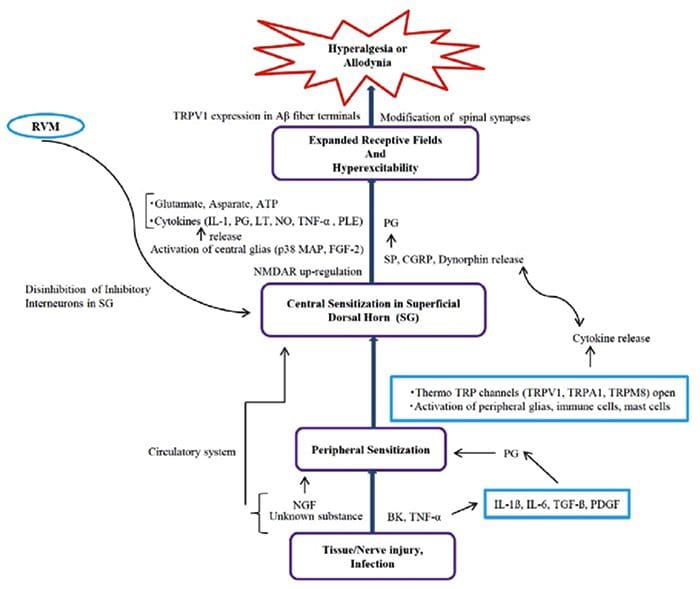
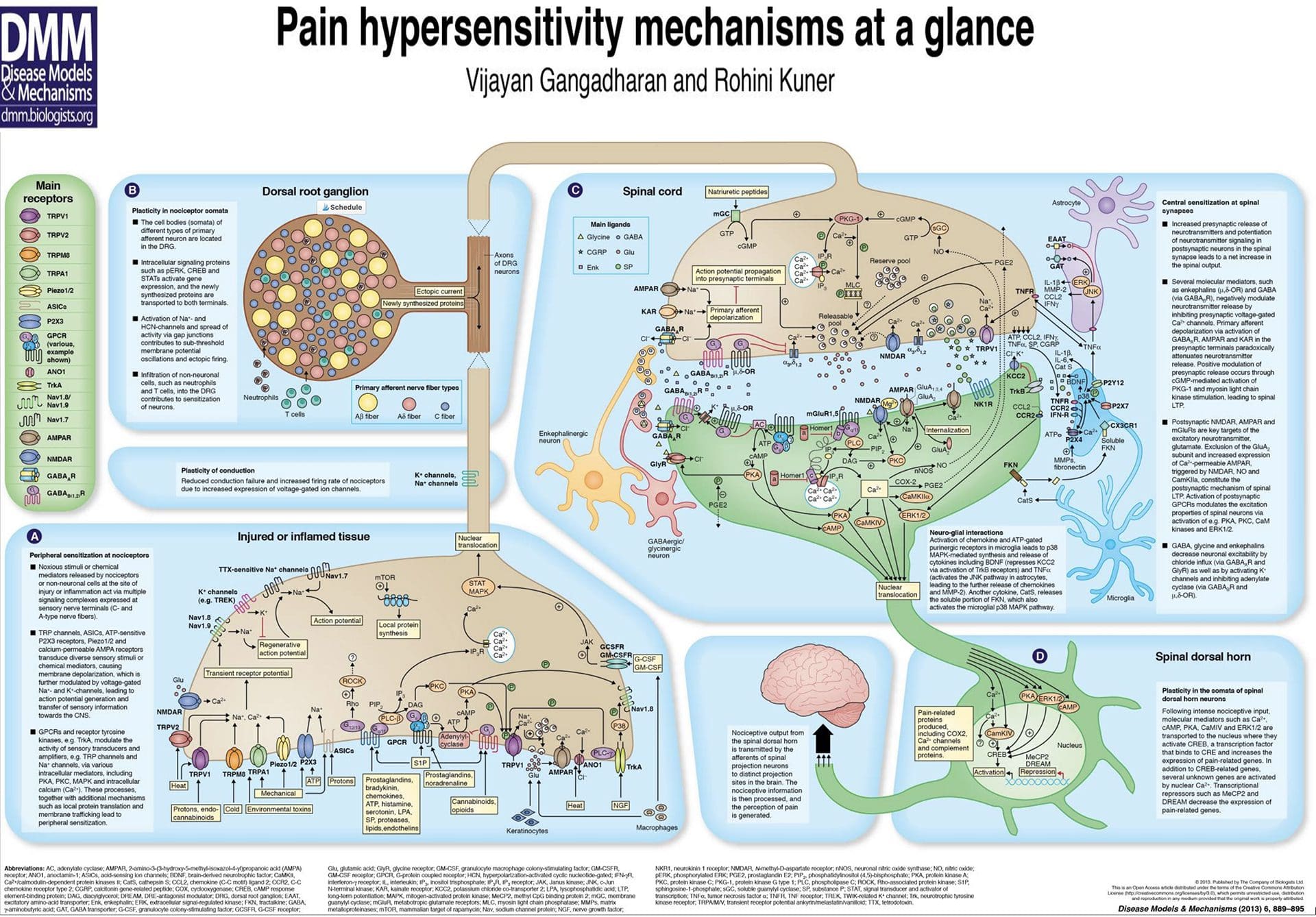
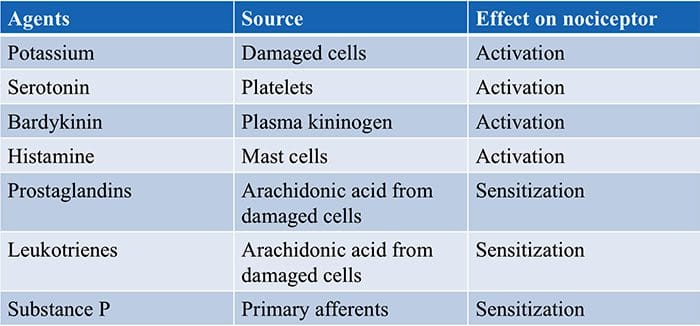
 Инфламаторна супа - Хипералгезија
Инфламаторна супа - Хипералгезија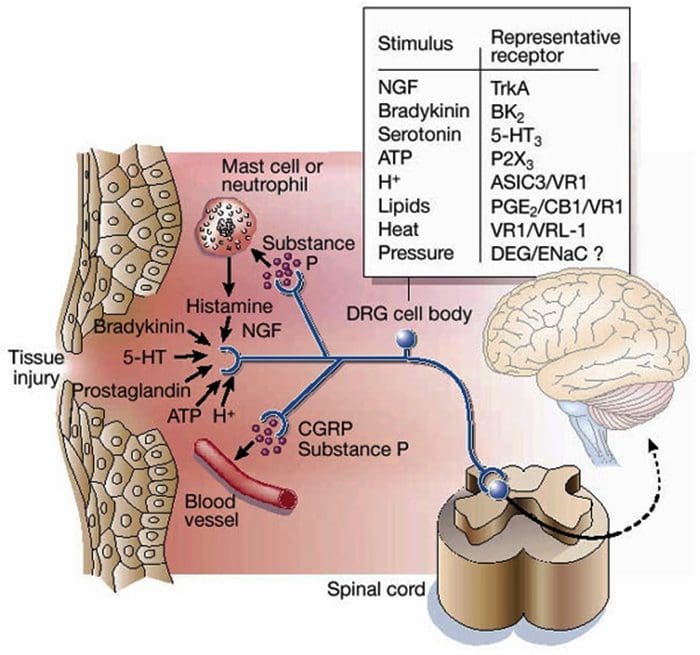
 Теорија бола контроле капије
Теорија бола контроле капије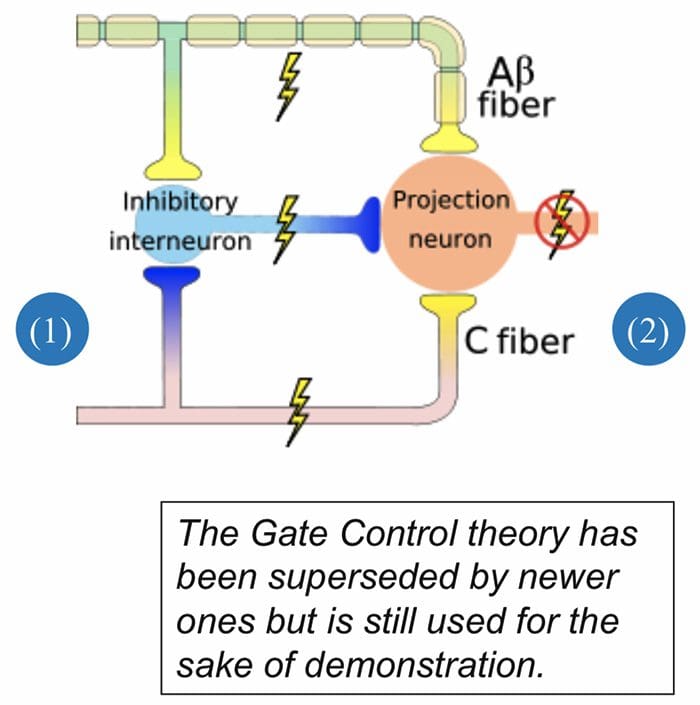
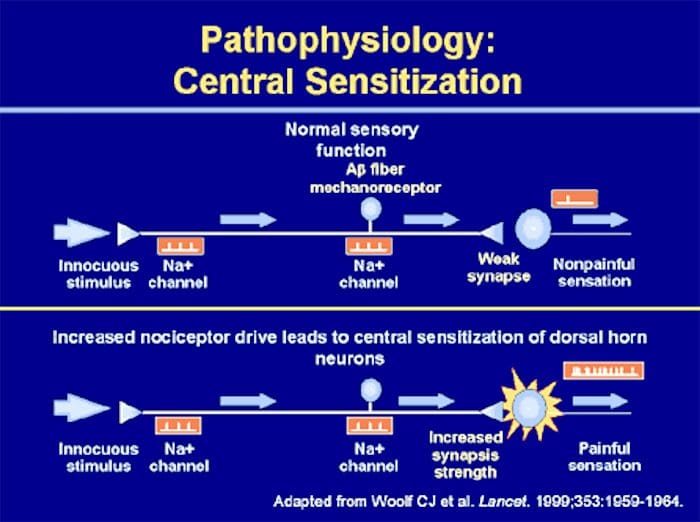
 Абнормалности система бола
Абнормалности система бола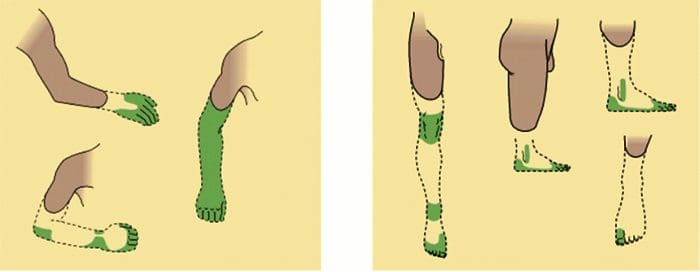 Периферна сензибилизација
Периферна сензибилизација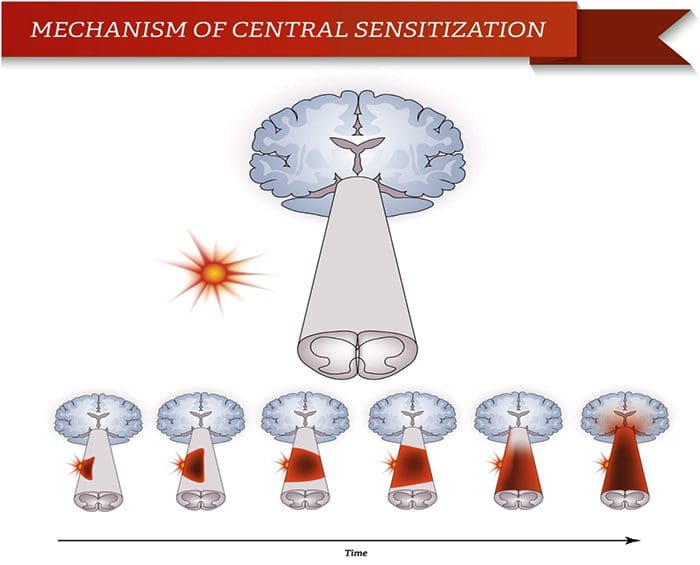
 Организација соматосензорног кортекса
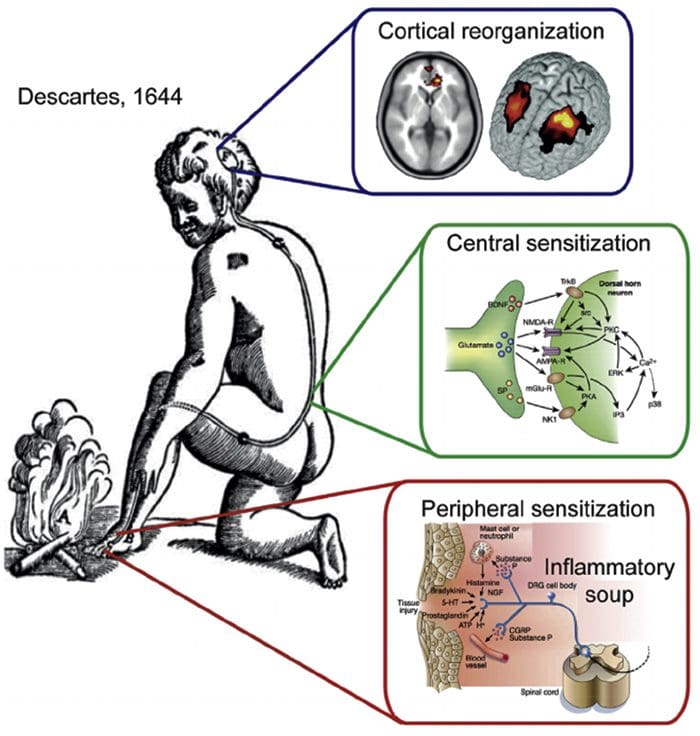
Организација соматосензорног кортекса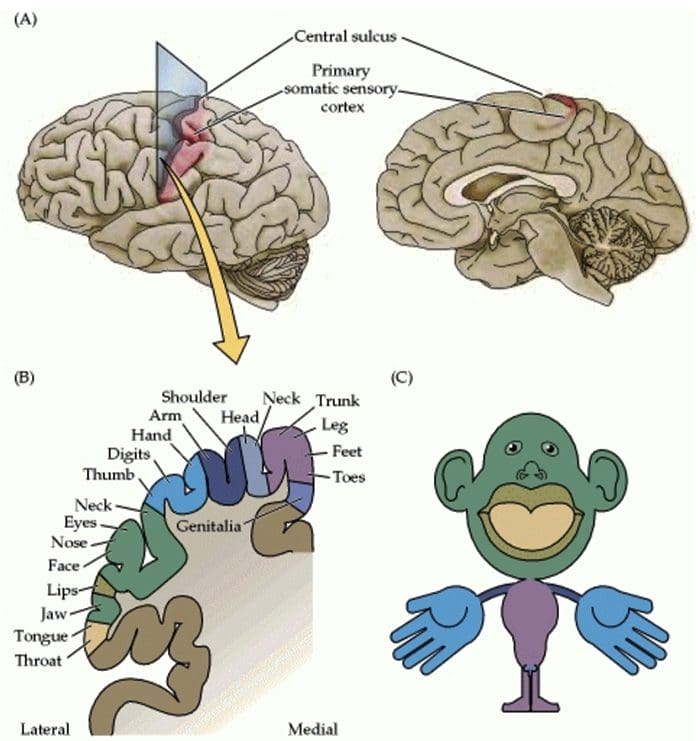 Кортикална реорганизација
Кортикална реорганизација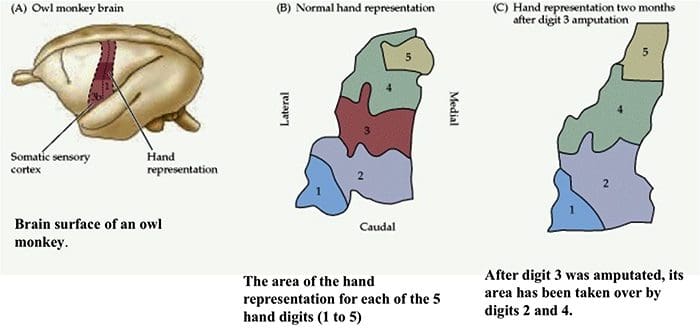

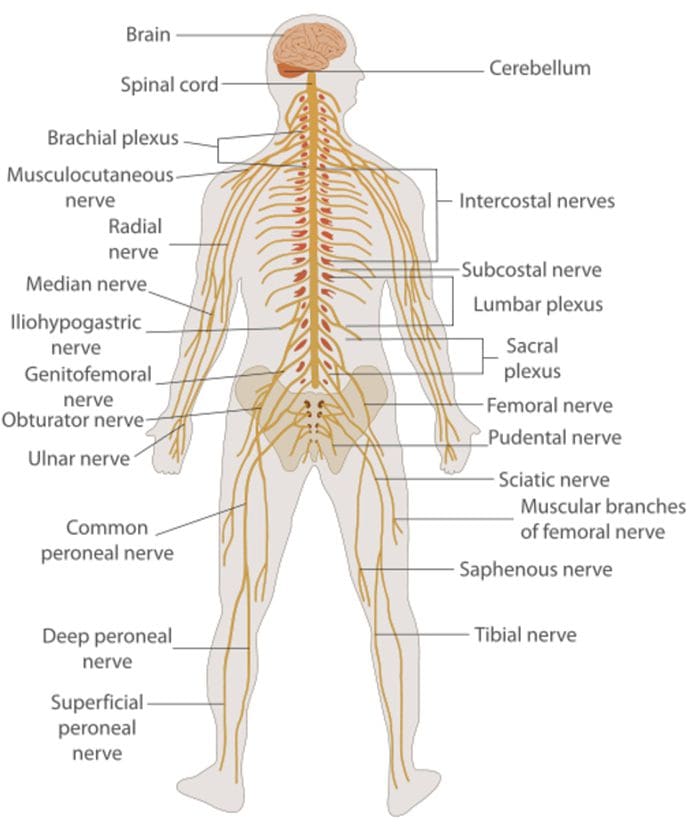
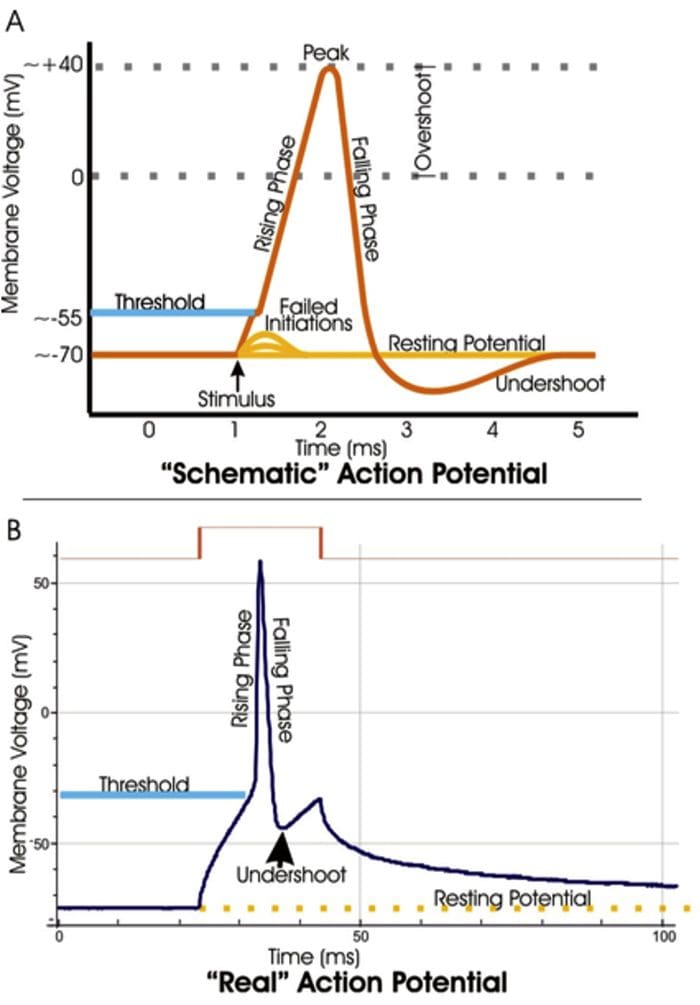
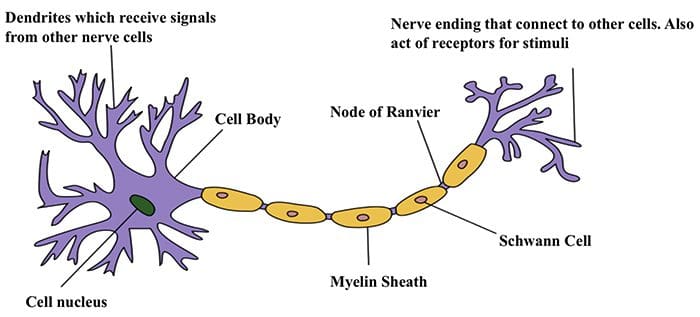 Комуникација између нервних ћелија
Комуникација између нервних ћелија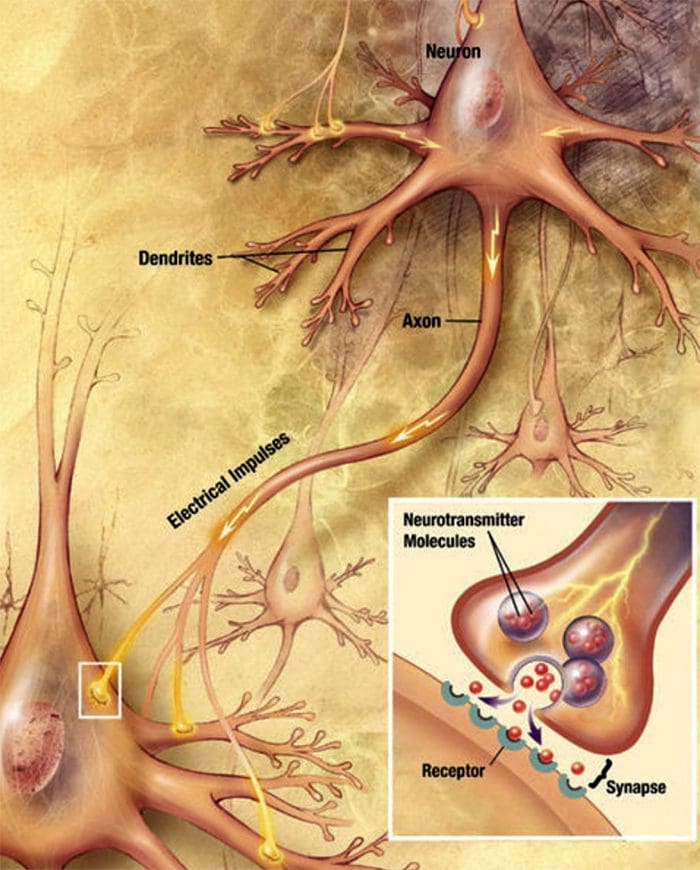 Нервне ћелије комуницирају са другим ћелијама ослобађањем хемикалије из нервних завршетака � Неуротрансмитери
Нервне ћелије комуницирају са другим ћелијама ослобађањем хемикалије из нервних завршетака � Неуротрансмитери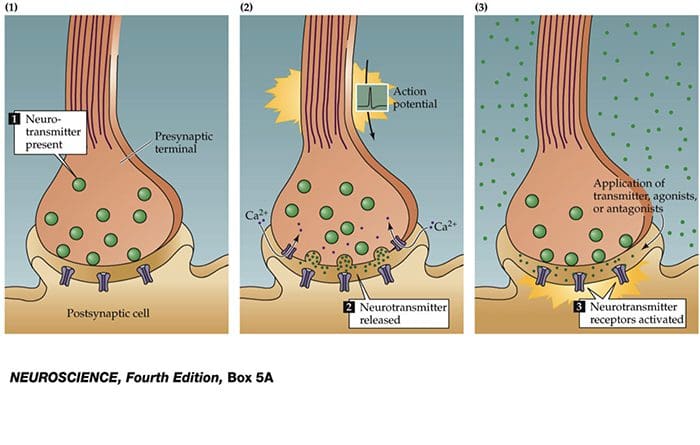
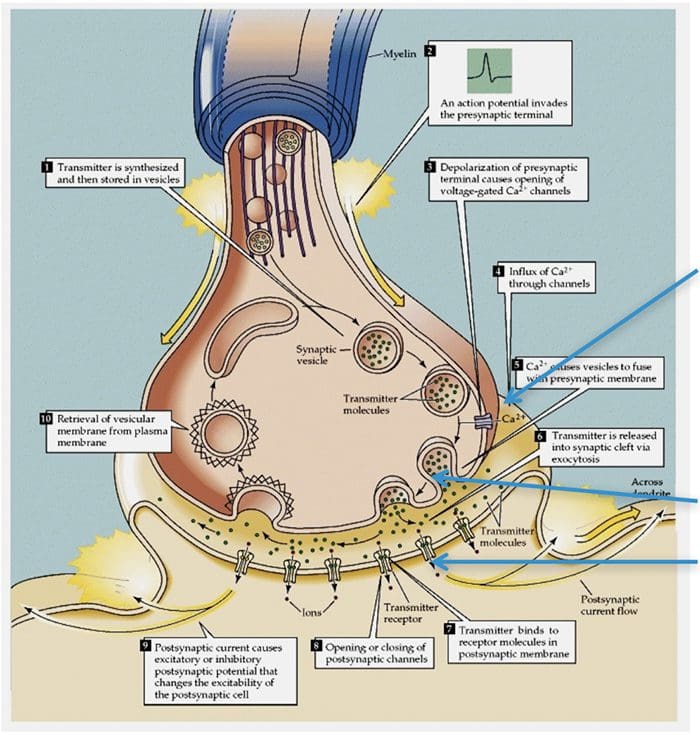
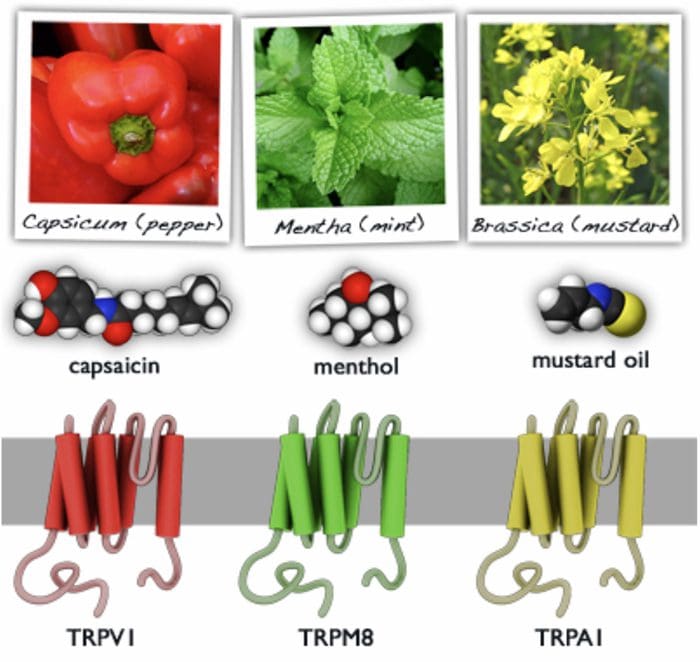
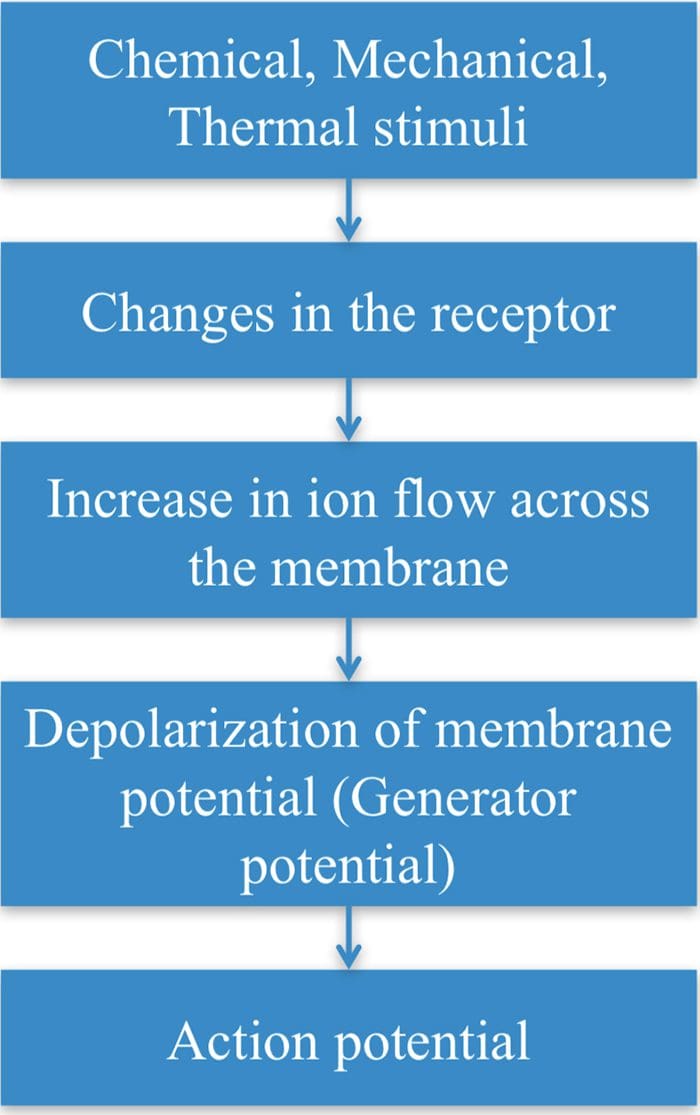 ТРП канали
ТРП канали