Сви смо као деца учили да постоји 5 чула: вид, укус, звук, мирис и додир. Прва четири чула користе јасне, различите органе, као што су очи, пупољци укуса, уши и нос, али како тачно чуло тела додирује? Додир се доживљава преко целог тела, како изнутра тако и споља. Не постоји један посебан орган који је одговоран за осећај додира. Уместо тога, постоје сићушни рецептори, или нервни завршеци, око целог тела који осећају додир тамо где се дешава и шаљу сигнале у мозак са информацијама о врсти додира који се десио. Пошто чуло укуса на језику детектује укус, механорецептори су жлезде у кожи и на другим органима које детектују осећај додира. Они су познати као механорецептори јер су дизајнирани да детектују механичке сензације или разлике у притиску.
Садржај
Улога механорецептора
Особа разуме да је доживела осећај када орган одговоран за откривање тог специфичног чула пошаље поруку мозгу, који је примарни орган који обрађује и распоређује све информације. Поруке се шаљу из свих делова тела у мозак преко жица које се називају неурони. Постоје хиљаде малих неурона који се гранају на све делове људског тела, а на крајевима многих од ових неурона су механорецептори. Да бисмо демонстрирали шта се дешава када додирнете објекат, користићемо пример.
Замислите да вам комарац слети на руку. Напон овог инсекта, тако лаган, стимулише механорецепторе у том делу руке. Ти механорецептори шаљу поруку дуж неурона са којим су повезани. Неурон се повезује све до мозга, који прима поруку да нешто додирује ваше тело на тачној локацији одређеног механорецептора који је послао поруку. Мозак ће деловати са овим саветом. Можда ће рећи очима да погледају регион руке која је открила потпис. А када очи кажу мозгу да је комарац на руци, мозак може рећи руци да га брзо одгурне. Тако функционишу механорецептори. Сврха чланка у наставку је да демонстрира, као и да детаљно продискутује функционалну организацију и молекуларне детерминанте механорецептора.
Чуло додира: Функционална организација и молекуларне детерминанте механосензитивних рецептора
Апстрактан
Кожни механорецептори су локализовани у различитим слојевима коже где детектују широк спектар механичких стимулуса, укључујући лагану четку, истезање, вибрације и штетни притисак. Ова разноврсност стимулуса је усклађена са разноликим низом специјализованих механорецептора који реагују на деформацију коже на специфичан начин и преносе ове стимулусе вишим можданим структурама. Студије о механорецепторима и генетски водљивим сензорним нервним завршецима почињу да откривају механизме чула додира. Рад у овој области пружио је истраживачима детаљније разумевање организације кола која лежи у основи перцепције додира. Нови јонски канали су се појавили као кандидати за трансдукционе молекуле, а својства механички затворених струја побољшала су наше разумевање механизама адаптације на тактилне стимулусе. Овај преглед наглашава напредак постигнут у карактеризацији функционалних својстава механорецептора у длакавој и голој кожи и јонским каналима који детектују механичке улазе и прилагођавају механорецептору облику.
Кључне речи: механорецептор, механосензитивни канал, бол, кожа, соматосензорни систем, додир
увод
Додир је детекција механичког стимулуса који утиче на кожу, укључујући безопасне и штетне механичке стимулусе. То је суштински смисао за опстанак и развој сисара и човека. Контакт чврстих предмета и течности са кожом даје неопходне информације централном нервном систему који омогућава истраживање и препознавање околине и покреће локомоцију или планирано кретање руке. Додир је такође веома важан за шегртовање, друштвене контакте и сексуалност. Чуло додира је најмање рањиво чуло, иако може бити искривљено (хиперестезија, хипоестезија) у многим патолошким стањима.1-3
Реакције на додир укључују веома прецизно кодирање механичких информација. Кожни механорецептори су локализовани у различитим слојевима коже где детектују широк спектар механичких стимулуса, укључујући светло четкицу, истезање, вибрације, отклон косе и штетни притисак. Ова разноврсност стимулуса је усклађена са разноликим низом специјализованих механорецептора који реагују на деформацију коже на специфичан начин и преносе ове стимулусе вишим можданим структурама. Соматосензорни неурони коже спадају у две групе: механорецептори ниског прага (ЛТМР) који реагују на бенигни притисак и механорецептори високог прага (ХТМР) који реагују на штетну механичку стимулацију. ЛТМР и ХТМР ћелијска тела се налазе унутар дорзалних ганглија корена (ДРГ) и кранијалних сензорних ганглија (тригеминални ганглији). Нервна влакна повезана са ЛТМР и ХТМР класификована су као А?-, А?- или Ц-влакна на основу њихових брзина проводљивости акционог потенцијала. Ц влакна су немијелинизирана и имају најспорије брзине проводљивости (~2 м/с), док А? и А? влакна су благо и јако мијелинизирана, показујући средње (~12 м/с) и брзе (~20 м/с) брзине проводљивости, респективно. ЛТМР се такође класификују као одговори који се споро или брзо прилагођавају (СА- и РА-ЛТМР) према њиховој стопи адаптације на трајни механички стимулус. Даље се разликују по кожним крајњим органима које инервирају и њиховим преферираним стимулусима.
Способност механорецептора да детектују механичке знакове ослања се на присуство јонских канала механотрансдуктора који брзо трансформишу механичке силе у електричне сигнале и деполаризују рецептивно поље. Ова локална деполаризација, названа рецепторски потенцијал, може да генерише акционе потенцијале који се шире ка централном нервном систему. Међутим, својства молекула који посредују у механотрансдукцији и прилагођавању механичким силама остају нејасна.
У овом прегледу дајемо преглед својстава механорецептора сисара у безопасном и штетном додиру на длакавој и голој кожи. Такође разматрамо недавна сазнања о својствима механички затворених струја у покушају да објаснимо механизам адаптације механорецептора. На крају, разматрамо недавни напредак постигнут у идентификацији јонских канала и повезаних протеина одговорних за генерисање механизованих струја.
Инноцуоус Тоуцх
ЛТМР-ови повезани са фоликулима косе
Фоликули длаке представљају мини органе који производе длаку и који детектују лагани додир. Влакна повезана са фоликулима длаке реагују на кретање косе и њен правац тако што испаљују низове акционих потенцијала на почетку и уклањању стимулуса. Они се брзо прилагођавају рецепторима.
Мачка и зец. У капуту мачака и зечева, фоликули длаке се могу поделити на три типа фоликула длаке, Довн длака, Гуард длака и Тилотрицхс. Длаке (поддлака, вуна, веллус)4 су најбројније, најкраће и најфиније длаке длаке. Таласасте су, безбојне и избијају у групама од две до четири длаке из заједничког отвора на кожи. Чуварске длаке (монотрицхс, оверхеарс, топхаир)4 су благо закривљене, пигментиране или непигментиране, и избијају појединачно из уста њихових фоликула. Тилотрихи су најмање бројни, најдуже и најдебље длаке.5,6 Пигментирани су или непигментирани, понекад и једно и друго и изникли су појединачно из фоликула који је окружен петљом капиларних крвних судова. Сензорна влакна која снабдевају фоликул длаке налазе се испод лојне жлезде и приписују се А? или А?-ЛТМР влакна.7
У блиској супротности са доњом длаком, одмах испод нивоа лојне жлезде налази се прстен копљастих пило-Руффини завршетака. Ови сензорни нервни завршеци су позиционирани у спиралном току око длаке унутар везивног ткива које формира фоликул длаке. Унутар фоликула длаке постоје и слободни нервни завршеци, неки од њих формирају механорецепторе. Често додирна тела (видети голу кожу) окружују вратни део тилотрих фоликула.
Својства мијелинизираних нервних завршетака у длакавој кожи мачака и зечева интензивно су истражена у периоду 1930–1970 (преглед у Хаманн, 1995).8 Занимљиво је да су Бровн и Игго проучавали 772 јединице са мијелинизираним аферентним нервним влакнима из мачјег нерава. и зец, класификовали су одговоре у три типа рецептора који одговарају покретима Довн длака (тип Д рецептора), Гуард длаке (тип Г рецептора) и Тилотрицх длаке (тип Т рецептора).9 Сви одговори аферентних нервних влакана су спојени у Рапидли Адаптинг рецептор типа И (РА И) насупрот Пацинијевом рецептору под називом РА ИИ. Механорецептори РА И детектују брзину механичког стимулуса и имају оштру границу. Не откривају температурне варијације. Бургесс ет ал. такође је описао рецептор поља који се брзо прилагођава и који оптимално реагује на мажење по кожи или померање неколико длачица, што се приписује стимулацији пило-Руффини завршетака. Ниједан одговор фоликула длаке није приписан активности Ц влакана.10
Мишеви. У дорзалној длакавој кожи мишева описана су три главна типа фоликула длаке: цик-цак (око 72%), шило/аушен (око 23%) и штитник или тилотрих (око 5%).11-14 цик-цак и шило/ ауцхенне фоликули длаке производе тање и краће длаке и повезани су са једном лојном жлездом. Заштитне или тилотричне длаке су најдуже од типова фоликула длаке. Одликује их велика сијалица за косу повезана са две лојне жлезде. Длаке штитника и шила/аушена су распоређене у итеративном, правилно распоређеном узорку, док цик-цак длаке густо насељавају подручја коже која окружују два већа типа фоликула длаке (Сл. 1 (А1, А2 и А3)].
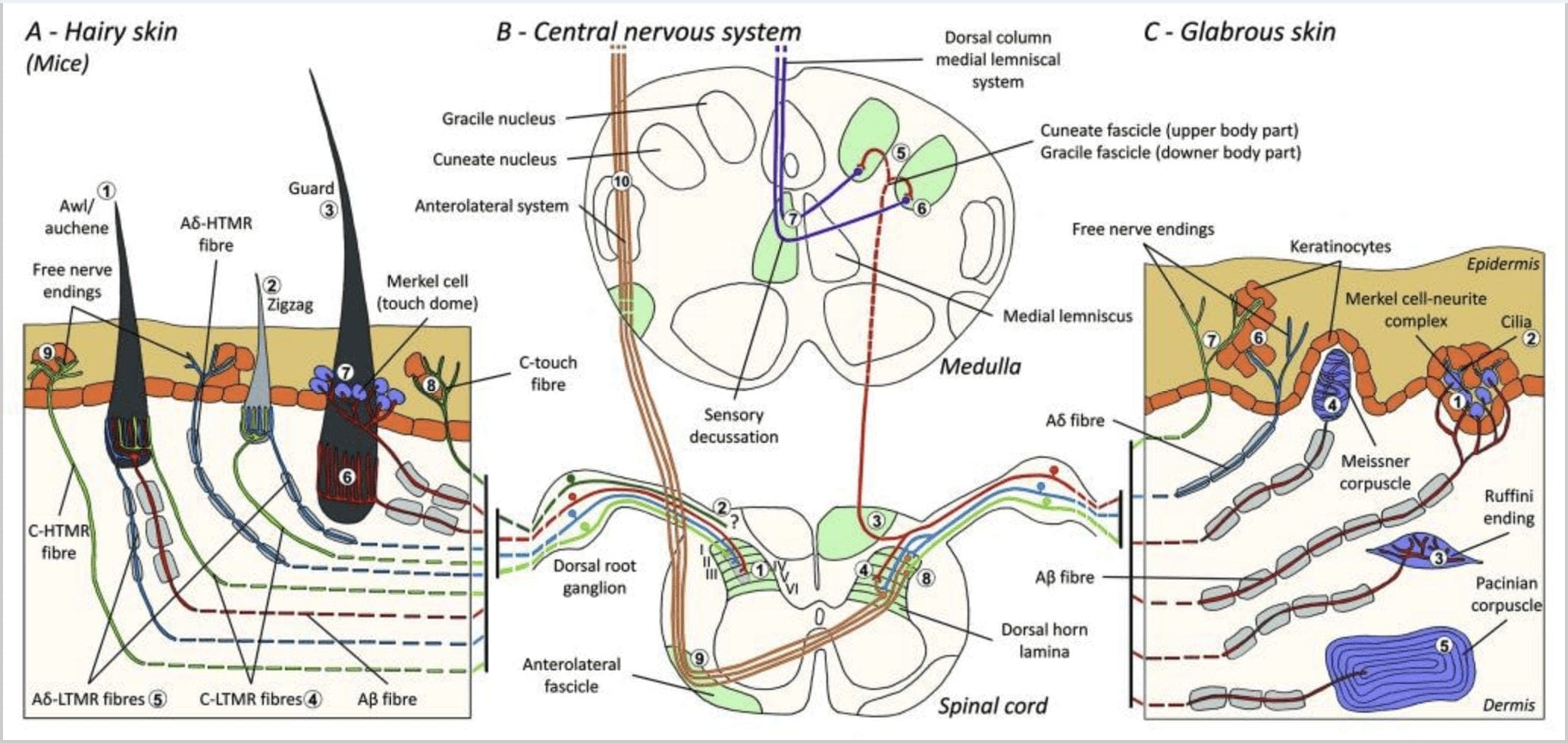
Слика КСНУМКС. Организација и пројекције кожних механорецептора. Код длакаве коже, лагана четка и додир се углавном детектују инервацијом око фоликула длаке: шило/ауцхенне (А1), цик-цак (А2) и штитник (А3). Авл/ауцхене длаке су троструко инервиране Ц-ЛТМР копљастим завршецима (А4), А?-ЛТМР и А? брзо прилагођавање-ЛТМР (А6). Цик-цак фоликули длаке су краће длаке и инервирају их и Ц-ЛТМР (А4) и А? -ЛТМР копљасти завршеци (А5). Најдужи заштитни фоликули длаке су инервирани А? брзо адаптирајући-ЛТМР уздужни ланцеолатни завршеци (А6) и повезани су са А? полако се прилагођава-ЛТМР завршетака додирне куполе (А7). Централне пројекције свих ових влакана завршавају се у различитим, али делимично преклапајућим ламинама дорзалног рога кичмене мождине (Ц-ЛТМР у ламини ИИ, А?-ЛТМР у ламини ИИИ и А?-ЛТМР у ламини ИВ и В). Пројекције ЛТМР-а које инервирају исте или суседне фоликуле длаке су поређане тако да формирају уски стуб у дорзалном рогу кичмене мождине (Б1 у сивој боји). Само код длакаве коже, субпопулација слободних завршетака Ц-влакна инервира епидермис и реагује на пријатан додир (А8). Ова Ц-тоуцх влакна не реагују на штетни додир и њихов пут још није познат (Б2). Код голе коже, безопасан додир је посредован са четири типа ЛТМР-а. Комплекс Меркелова ћелија-неурит налази се у базалном слоју епидермиса (Ц1). Овај механорецептор се састоји од аранжмана између многих Меркелових ћелија и увећаног нервног терминала из једног А? влакно. Меркелове ћелије показују процесе попут прстију који контактирају кератиноците (Ц2). Руффини завршетак је локализован у дермису. То је танки инкапсулирани сензорни завршеци у облику цигаре повезани са А? влакна (Ц3). Мајснерово тело повезано са А? нервног завршетка и налази се у дермалним папилама. Овај инкапсулирани механорецептор се састоји од збијених потпорних ћелија распоређених као хоризонталне ламеле окружене везивним ткивом (Ц4). Пацинијево тело је дубљи механорецептор. Један једини А? немијелинизирани нервни завршетак завршава се у центру овог великог јајоликог корпускула сачињеног од концентричних ламела. Пројекције ових А?-ЛТМР влакана у кичменој мождини подељене су у две гране. Главна централна грана (Б3) уздиже се у кичмену мождину у ипсилатералном дорзалном делу формирајући клинасте или грацилне фасцикуле (Б5) на нивоу медуле где примарни аференти праве своју прву синапсу (Б6). Секундарни неурони праве сензорни пречник (Б7) да би формирали тракт на медијалном лемнискусу који се пење кроз мождано стабло до средњег мозга, тачније у таламусу. Секундарна грана ЛТМР завршава се у дорзалном рогу у ламини ИИ, ИВ, В и омета преношење бола (Б4). Штетан додир се детектује слободним нервним завршецима у епидермису и длакаве (А9) и голе коже (Ц7). Ови механорецептори су завршетак А?-ХТМР и Ц-ХТМР у блиском контакту са суседним кератиноцитима (Ц6). Аа-хТМР завршава у ламини И и В; Ц-ХТМР завршава у ламини И и ИИ (Б8). На нивоу дорзалног рогова кичмене мождине, примарни аферентни ХТМР праве синапсе са секундарним неуронима који прелазе средњу линију и пењу се до више структуре мозга у антеролатералном фасцикулу (Б9, Б10).
Недавно су Гинти и сарадници користили комбинацију молекуларно-генетског обележавања и приступа соматотопског ретроградног праћења да би визуелизовали организацију периферних и централних аксоналних завршетака ЛТМР-а код мишева.15 Њихови налази подржавају модел у којем су индивидуалне карактеристике сложеног тактилног стимулуса. екстрахује три типа фоликула длаке и преноси преко активности јединствених комбинација А?-, А?- и Ц- влакана до дорзалног рога.
Они су показали да генетско обележавање неурона позитивних на тирозин хидроксилазу (ТХ+) ДРГ карактерише популацију непептидергичних сензорних неурона малог пречника и омогућава визуализацију Ц-ЛТМР периферних завршетака у кожи. Изненађујуће, откривено је да се аксонске гране појединачних Ц-ЛТМР формирају и формирају уздужне копљасте завршетке који су блиско повезани са цик-цак (80% завршетака) и шилом/аушеном (20% завршетака), али не и фоликулима длаке богатим тилотријем [Сл. 1 (А4)]. Дуго се сматрало да уздужни ланцеолатни завршеци припадају искључиво А?-ЛТМР и стога је било неочекивано да ће завршеци Ц-ЛТМР формирати уздужне копљасте завршетке.15 Ови Ц-ЛТМР имају средњу адаптацију у поређењу са споро и брзо прилагођавајућим завршецима. мијелинизовани механорецептори [Сл. 2 (Ц1)].
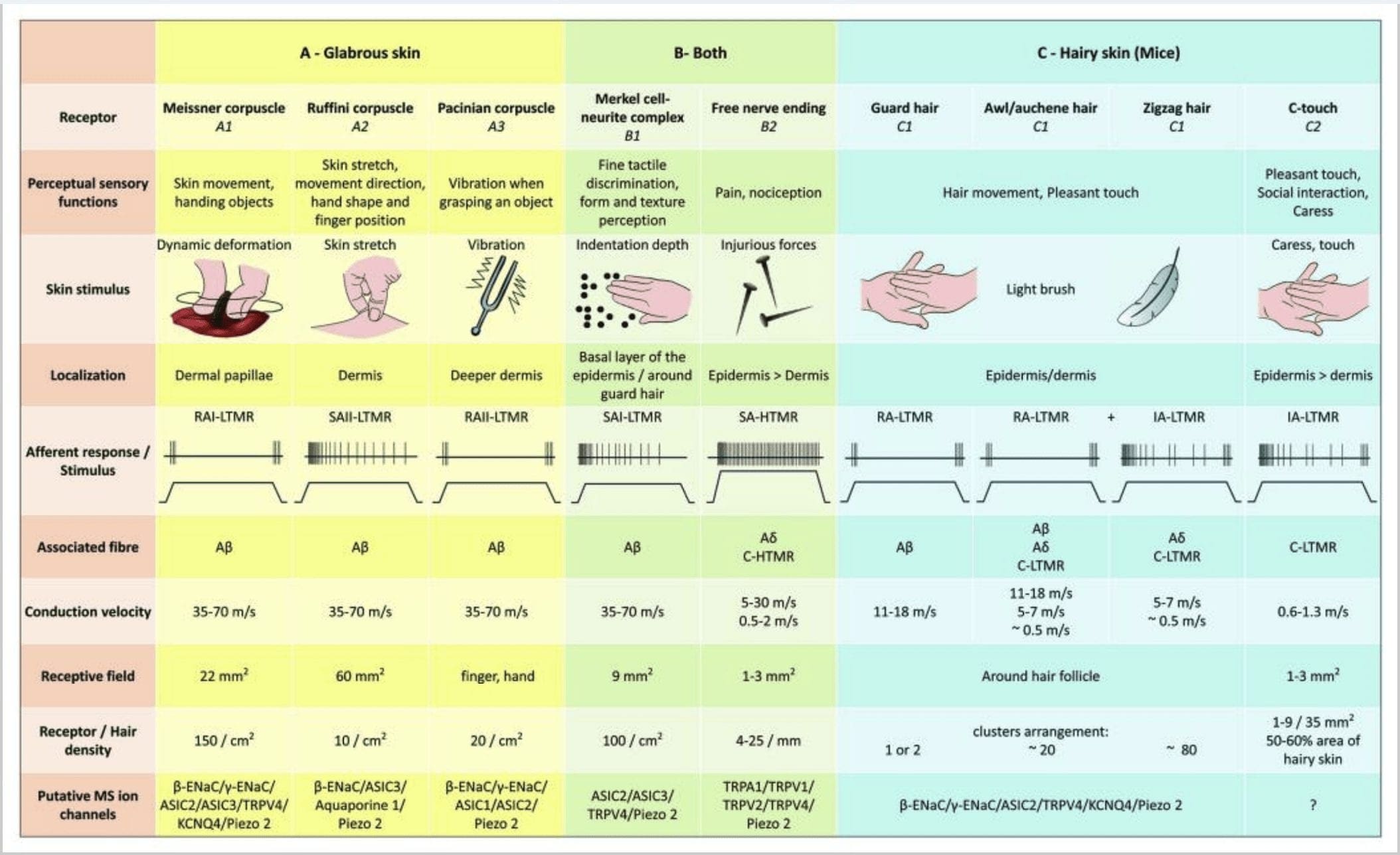
Слика КСНУМКС. Тактилни рецептори код сисара: Кожни тактилни рецептори се разликују у нешкодљив додир подржан вишеструким рецепторима са ниским механичким прагом (ЛТМР) у голој и длакавој кожи и штетни додир подржан рецепторима високог механичког прага (ХТМР). Они чине слободне нервне завршетке који се завршавају углавном у епидермису. (А) Глаброзна кожа. А1: Мајснерова ћелија детектују кретање коже и клизање предмета у руци. Важни су за преношење предмета и спретност. Рецептори се брзо прилагођавају стимулусу, повезани су са А? влакна и ретко до Ц влакна и имају велико поље рецептора. А2: Руффини корпускуле детектују истезање коже и важне су за откривање положаја прста и предмета који рукују. Рецептор се полако прилагођава стимулусу и одржава активност све док се стимулус примењује. Рецептори су повезани на А? влакна и имају велико рецептивно поље. А3: Пацинијана тела су дубље у дермису и детектују вибрације. Рецептори су повезани на А? влакна; брзо се прилагођавају стимулансу и имају највеће рецептивно поље. (Б) Цела кожа. Б1: Комплекси Меркел-ћелија присутни су и у голој кожи и око косе. Густо су изражени у руци и важни су за перцепцију текстуре и најфиније разликовање две тачке. Они су одговорни за прецизност прстију. Рецептори су повезани на А? влакна; полако се прилагођавају стимулансу и имају кратко рецептивно поље. Б2: ХТМР штетни на додир са веома спором адаптацијом на стимулус, тј. активни све док се примењује ноцицептивни стимулус. Настају слободним нервним завршетком А? и Ц-влакна повезана са кератиноцитима. (Ц) Длакава кожа. Ц1: Фоликули длаке су повезани са различитим типовима косе. Код мишева Гуард длаке су дуже и ретко изражене, шило/ауцхенне су средње величине, а цик-цак су најмања и најгушће изражена длака. Они су повезани са А? влакна али и на А? и Ц-ЛТМР влакна за шило/ауцхенне и цицак косу. Они детектују кретање косе, укључујући пријатан додир током миловања. Они се брзо или са средњом кинетиком прилагођавају на стимулус. Ц2: Ц-тоуцх нервни завршеци одговарају подтипу краја Ц влакана са слободним завршетком који карактерише низак механички праг. Они би требало да кодирају пријатан осећај изазван миловањем. Умерено се прилагођавају стимулансу и имају кратко рецептивно поље. Претпостављени механосензитивни (МС) јонски канали експримирани у различитим тактилним рецепторима су назначени у складу са прелиминарним подацима и сумирају тренутну хипотезу која се процењује.
Друга велика идентификована популација тиче се А?-ЛТМР завршетака у Авл/Ауцхенне и цик-цак фоликулима које треба упоредити са Довн фоликулом длаке који је опширно проучаван код мачака и зечева. Гинти и сарадници су показали да се ТркБ изражава на високим нивоима у подскупу ДРГ неурона средњег пречника. Интрацелуларни снимци коришћењем ек виво препарата коже и нерава означених влакана открили су да показују физиолошка својства влакана која су претходно проучавана код мачака и зечева: изузетна механичка осетљивост (Фон Фрејев праг < 0.07 мН), брзо прилагођавање одговора на стимулусе изнад прага, средња проводљивост брзинама (5.8 × 0.9 м/с) и уским несавијеним сома шиљцима.15 Ови А?-ЛТМР формирају уздужне копљасте завршетке повезане са скоро сваким цик-цак и шилом/аушеном фоликулом длаке на трупу [Сл. 1 (А5)].
Коначно, показали су да су периферни завршеци брзог прилагођавања А? ЛТМР формирају уздужне копљасте завршетке повезане са штитницима (или тилотрихом) и фоликулима длаке са шилом/аушеном [Сл. 1 (А6)].15 Поред тога, длаке Гарде су такође повезане са комплексом Меркелове ћелије који формира куполу на додир повезану са А? полако прилагођавајући ЛТМР [Сл. 1 (А7)].
Укратко, практично сви цик-цак фоликули длаке су инервирани и Ц-ЛТМР и А?-ЛТМР ланцеолатним завршецима; А? брзо адаптирајући-ЛТМР, А?-ЛТМР и Ц-ЛТМР копљасти завршеци; Чуварске фоликуле длаке инервира А? брзо прилагођавање-ЛТМР уздужни ланцеолатни завршеци и интеракцију са А? полако се прилагођава-ЛТМР завршетака додирне куполе. Дакле, сваки мишји фоликул длаке добија јединствене и непроменљиве комбинације ЛТМР завршетака које одговарају неурофизиолошки различитим механосензорним крајњим органима. Узимајући у обзир итеративни распоред ова три типа косе, Гинти и сарадници предлажу да се длакава кожа састоји од итеративног понављања периферне јединице која садржи: (1) једну или две централно лоциране заштитне длаке, (2) ~20 околних шила/ауцхенне длака и (3 ) ~80 испреплетених цик-цак власи [сл. 2 (Ц1)].
Пројекција кичмене мождине. Централне пројекције А? брзо адаптирајући ЛТМР, А?-ЛТМР и Ц-ЛТМР завршавају се у различитим, али делимично преклапајућим ламинама (ИИ, ИИИ, ИВ) дорзалног рога кичмене мождине. Поред тога, централни терминали ЛТМР-а који инервирају исте или суседне фоликуле длаке унутар периферне ЛТМР јединице су поравнати да формирају уски ЛТМР стуб у дорзалном рогу кичмене мождине [Сл. 1 (Б1)]. Стога се чини вероватним да клин или стуб соматотопски организованих примарних сензорних аферентних завршетака у дорзалном рогу представља поравнање централних пројекција А?-, А?- и Ц-ЛТМР које инервирају исту периферну јединицу и откривају механичке стимуланси који делују на исту малу групу фоликула длаке. На основу броја заштитних, шил/аушена и цик-цак длака трупа и удова и бројева сваког ЛТМР подтипа, Гинти и сарадници процењују да мишји дорзални рог садржи 2,000 × 4,000 ЛТМР колона, што одговара приближном броју колона на периферији ЛТМР јединице.15
Штавише, аксони ЛТМР подтипова су блиско повезани један са другим, имају испреплетене пројекције и интердигиталне ланцеолатне завршетке који инервирају исти фоликул длаке. Поред тога, пошто три типа фоликула длаке показују различите облике, величине и ћелијске композиције, они ће вероватно имати различита својства подешавања скретања или вибрација. Ови налази су у складу са класичним неурофизиолошким мерењима код мачке и зеца који показују да је А? РА-ЛТМР и А?-ЛТМР се могу различито активирати скретањем различитих типова фоликула длаке.16,17
У закључку, додир у длакавој кожи је комбинација: (1) релативног броја, јединствене просторне дистрибуције и различитих морфолошких и дефлекцијских својстава три типа фоликула длаке; (2) јединствене комбинације завршетака подтипа ЛТМР повезаних са сваким од три типа фоликула длаке; и (3) различите осетљивости, брзине проводљивости, шеме шиљака и својства прилагођавања четири главне класе ЛТМР-а повезаних са фоликулом длаке који омогућавају механосензорном систему длакаве коже да извуче и пренесе у ЦНС сложене комбинације квалитета које дефинишу додирнути.
ЛТМР-ови слободних нервних завршетака
Генерално, крајеви без Ц-влакана у кожи су ХТМР-ови, али субпопулација Ц-влакана не реагује на штетни додир. Ова подскупина аферената тактилних Ц-влакна (ЦТ) представља посебан тип немијелинизираних механорецептивних јединица ниског прага који постоје у длакавој, али не и голој кожи људи и сисара [Сл. 1 (А8)].18,19 ЦТ су генерално повезани са перцепцијом пријатне тактилне стимулације у контакту тела.20,21
ЦТ аференти реагују на силе удубљења у опсегу 0.3-2.5 мН и стога су осетљиви на деформацију коже као и многи А? аференти.19 Карактеристике адаптације ЦТ аферената су стога средње у поређењу са споро и брзо адаптирајућим мијелинизованим механорецепторима. Рецептивна поља људских ЦТ аферената су отприлике округлог или овалног облика. Поље се састоји од једне до девет малих тачака које реагују распоређене на површини до 35 мм2.22 Хомолог рецептори миша су организовани у шаблону дисконтинуираних мрља које покривају око 50% површине у длакавој кожи [Сл. 60 (Ц2)].2
Докази код пацијената који немају мијелинизоване тактилне аференте указују на то да сигнализација у ЦТ влакнима активира острвски кортекс. Пошто је овај систем лош у кодирању дискриминативних аспеката додира, али је добро прилагођен за кодирање спорог, нежног додира, ЦТ влакна у длакавој кожи могу бити део система за обраду пријатних и друштвено релевантних аспеката додира.24 Активација ЦТ влакана такође може бити имају улогу у инхибицији бола и недавно је предложено да запаљење или траума могу променити осећај који преносе Ц-влакна ЛТМР од пријатног додира до бола.25,26
Којим путем путују ЦТ-аференти још није познато [Сл. 1 (Б2)], али су документовани тактилни инпути ниског прага у спиноталамичке пројекцијске ћелије,27 што даје веродостојност извештајима о суптилним, контралатералним дефицитима детекције додира код људских пацијената након уништења ових путева након процедура хордотомије.28
ЛТМР у глаткој кожи
Меркелова ћелија-неурит комплекси и додирна купола. Меркел (1875) је прва дала хистолошки опис кластера епидермалних ћелија са великим лобулираним језгрима, успостављајући контакт са претпостављеним аферентним нервним влакнима. Претпоставио је да су подвргавали чулу додира називајући их Тастзеллен (тактилне ћелије). Код људи, комплекси Меркелове ћелије неурита су обогаћени деловима коже осетљивим на додир, налазе се у базалном слоју епидермиса у прстима, уснама и гениталијама. Они такође постоје у длакавој кожи мање густине. Комплекс неуритних ћелија Меркелове ћелије се састоји од Меркелове ћелије у блиској супротности са увећаним нервним терминалом из једног мијелинизованог А? влакно [Сл. 1 (Ц1)] (преглед у Халати и сарадницима).29 На епидермалној страни Меркелова ћелија показује прстасте процесе који се протежу између суседних кератиноцита [Сл. 1 (Ц2)]. Меркелове ћелије су епидермалне ћелије изведене из кератиноцита.30,31 Термин додирне куполе је уведен да именује велику концентрацију комплекса Меркелових ћелија у длакавој кожи мачје предње шапе. Додирна купола може имати до 150 Меркелових ћелија инервираних једним А?-влакном, а код људи поред А?-влакна, А? а редовно су била присутна и Ц-влакна.32-34
Стимулација неуритних комплекса Меркелове ћелије доводи до споро прилагођавајућих одговора типа И (СА И), који потичу из пунктираних рецептивних поља са оштрим границама. Нема спонтаног пражњења. Ови комплекси реагују на дубину удубљења коже и имају највећу просторну резолуцију (0.5 мм) кожних механорецептора. Они преносе прецизну просторну слику тактилних стимулуса и претпоставља се да су одговорни за дискриминацију облика и текстуре [Сл. 2 (Б1)]. Мишеви лишени Меркелових ћелија не могу да открију текстуриране површине својим стопалима док то раде помоћу бркова.35
Да ли су Меркелова ћелија, сензорни неурон или оба места механотрансдукције још увек је предмет расправе. Код пацова, фототоксично уништавање Меркелових ћелија укида СА И одговор.36 Код мишева са генетски потиснутим Меркел ћелијама, СА И одговор забележен ин ек виво препарат коже/нерва је потпуно нестао, показујући да су Меркелове ћелије потребне за правилно кодирање Меркелове. реакције рецептора.37 Међутим, механичка стимулација изолованих Меркел ћелија у култури моторним притиском не генерише механички управљане струје.38,39 Кератиноцити могу играти важну улогу у нормалном функционисању неуритног комплекса Меркел ћелија. Процеси налик прстима Меркелове ћелије могу се кретати са деформацијом коже и кретањем ћелија епидермиса, а ово може бити први корак механичке трансдукције. Јасно је да услови потребни за проучавање механо-осетљивости Меркелових ћелија тек треба да буду успостављени.
Руффини завршници. Руффини завршници су танки капсулирани сензорни завршеци у облику цигаре повезани са А? Крајеви нерава. Руффини завршеци су мали цилиндри везивног ткива распоређени дуж дермалних колагенских нити које снабдевају једно до три мијелинизована нервна влакна пречника 4 м. До три цилиндра различите оријентације у дермису могу се спојити и формирати један рецептор [Сл. 6 (Ц1)]. Структурно, Руффини завршеци су слични Голгијевим тетивним органима. Они су широко изражени у дермису и идентификовани су као кожни механорецептори који се споро прилагођавају типа ИИ (СА ИИ). У позадини спонтане нервне активности, полако прилагођавајући се регуларни пражњење се изазива механичком стимулацијом која се одржава управном ниском силом или ефикасније растезањем коже. СА ИИ одговор потиче из великих рецептивних поља са нејасним границама. Руффини рецептори доприносе перцепцији правца кретања објекта кроз образац истезања коже [Сл. 3 (А2)].
Код мишева, СА И и СА ИИ одговори се могу електрофизиолошки раздвојити у ек виво препарацији нерва-коже.40 Нандасена и сарадници су известили о имунолокализацији аквапорина 1 (АКП1) у пародонталним Руффини завршецима секутића пацова што сугерише да је АКП1 укључен у одржавање денталне осмотске равнотеже неопходне за механотрансдукцију.41 Пародонтални Руффини завршеци су такође изразили претпостављени механосензитивни јонски канал АСИЦ3.42
Мајснерова тела. Мајснерова тјелешца су локализована у дермалним папилама голе коже, углавном на длановима и табанима, али и на уснама, језику, лицу, брадавицама и гениталијама. Анатомски, састоје се од инкапсулираног нервног завршетка, при чему је капсула направљена од спљоштених потпорних ћелија распоређених као хоризонталне ламеле уграђене у везивно ткиво. Постоји једно нервно влакно А? аференти повезани по корпускулу [Сл. 1 (Ц4)]. Свака физичка деформација корпускула покреће талас акционих потенцијала који брзо престају, односно брзо се прилагођавају рецепторима. Када се стимулус уклони, тело враћа свој облик и при томе производи још један талас акционих потенцијала. Због своје површне локације у дермису, ова корпускула селективно реагују на покрете коже, тактилну детекцију клизања и вибрације (20-40 Хз). Они су осетљиви на динамичку кожу – на пример, између коже и предмета којим се рукује [Сл. 2 (А1)].
Пацинијана тела. Пацинијева телашца су дубљи механорецептори коже и најосетљивији су инкапсулирани кожни механорецептор кретања коже. Ова велика јајолична телашца (дужине 1 мм) направљена од концентричних ламела влакнастог везивног ткива и фибробласта обложених равним модификованим Швановим ћелијама су изражена у дубоком дермису.43 У центру тела, у шупљини испуњеној течношћу која се зове унутрашња сијалица. , завршава један једини А? аферентни немијелинизовани нервни завршетак [Сл. 1 (Ц5)]. Имају велико рецептивно поље на површини коже са посебно осетљивим центром. Развој и функција неколико типова механорецептора који се брзо прилагођавају поремећени су код ц-Маф мутантних мишева. Нарочито су Пацинијана телашца јако атрофирана.44
Пацинијево тело показује веома брзу адаптацију као одговор на удубљење коже, брзо прилагођавање ИИ (РА ИИ) нервног пражњења које је способно да прати високу фреквенцију вибрационих стимулуса и омогућава перцепцију удаљених догађаја путем пренетих вибрација.45 Пацинијево тело аференти реагују на трајно удубљење са пролазном активношћу на почетку и отклањању стимулуса. Називају се и детектори убрзања јер могу да открију промене у јачини стимулуса и, ако се промени брзина промене стимулуса (као што се дешава код вибрација), њихов одговор постаје пропорционалан овој промени. Пацинијана телашца осећају грубе промене притиска и пре свега вибрације (150-300 Хз), које могу да открију чак и на центиметрима удаљености [Сл. 2 (А3)].
Тонични одговор је примећен у декапсулираном Пацинијевом телу.46 Поред тога, нетакнута Пацинијанова корпускула реагују континуираном активношћу током константних стимуланса удубљења, без промене механичких прагова или фреквенције одговора када је сигнализација посредована ГАБА блокирана између ламелатне глије и нервног завршетка.47 Дакле, не-неуронске компоненте Пацинијевог корпускула могу имати двоструку улогу у филтрирању механичког стимулуса као и у модулацији својстава одговора сензорног неурона.
Пројекције кичмене мождине. Пројекције А?-ЛТМР у кичменој мождини подељене су у две гране. Главна централна грана се уздиже у кичменој мождини у ипсилатералним дорзалним стубовима до нивоа грлића материце (Сл. 1 (Б3)]. Секундарне гране завршавају се у дорзалном рогу у ламинама ИВ и ометају пренос бола, на пример. Ово може ублажити бол као део контроле капије [Сл. 1 (Б4)].48
На нивоу грлића материце, аксони главне гране се одвајају у два тракта: средњи тракт обухвата грацилну фасциклу која преноси информације из доње половине тела (ноге и труп), а спољни тракт обухвата клинасти фасцикул који преноси информације из горње половине тела (руке и труп) [Сл. 1 (Б5)].
Примарни тактилни аференти праве своју прву синапсу са неуронима другог реда у медули где влакна из сваког тракта синапсе у истоименом језгру: синапса аксона грацилног фасцикулуса у грацилном језгру и синапса аксона клинастог аксона у клинастом језгру [Сл. 1 (Б6)]. Неурони који примају синапсу обезбеђују секундарне аференте и одмах прелазе средњу линију да би формирали тракт на контралатералној страни можданог стабла – медијални лемнискус – који се пење кроз мождано стабло до следеће релејне станице у средњем мозгу, тачније у таламусу (Сл. . 1 (Б7)].
Молекуларна спецификација ЛТМР. Молекуларни механизми који контролишу рану диверсификацију ЛТМР-а недавно су делимично разјашњени. Боуране и сарадници су показали да неуронске популације које експримирају Рет рецептор тирозин киназе (Рет) и његов ко-рецептор ГФР?2 код Е11�13 ембрионалних мишева ДРГ селективно коекспримирају фактор транскрипције Мафа.49,50 Ови аутори показују да Мафа/ Рет/ГФР?2 неурони су предодређени да постану три специфична типа ЛТРМ-а при рођењу: неурони СА1 који инервирају комплексе Меркел-ћелија, неурони који се брзо прилагођавају који инервирају Мајснерово тело и брзо адаптирајући аференти (РА И) који формирају копљасте завршетке око фоликула длаке. Гинти и сарадници такође извештавају да ДРГ неурони који експримирају рани-Рет брзо прилагођавају механорецепторе из Мајснерових телаша, Пацинијевих телаша и ланцетастих завршетака око фоликула длаке.51 Они инервирају дискретне циљне зоне унутар грацилног и клинастог језгра, откривајући механоспецифични образац аксонске пројекције неурона унутар можданог стабла.
Истраживање механорецептора људске коже. Техника "микронеурографије" коју су описали Хагбартх и Валлбо 1968. године примењена је за проучавање понашања пражњења појединачних људских механичко осетљивих завршетака који снабдевају мишиће, зглобове и кожу (видети преглед Мацефиелд, 2005).52,53 Већина микронеурографије људске коже студије су карактерисале физиологију тактилних аферената у голој кожи шаке. Снимци микроелектрода са средњих и улнарних нерава код људских субјеката су открили осећај додира који генерише четири класе ЛТМР-а: Мајснерови аференти су посебно осетљиви на лагане ударце по кожи, реагујући на локалне силе смицања и почетна или очигледна клизања унутар рецептивног поља. Пацинијанови аференти су изузетно осетљиви на брзе механичке транзијенте. Аференти снажно реагују на дување преко рецептивног поља. Пацинијево тело које се налази у цифри обично ће реаговати на тапкање по столу који подржава руку. Меркелови аференти карактеристично имају високу динамичку осетљивост на стимулусе удубљења примењене на дискретну област и често реагују са искљученим пражњењем током ослобађања. Иако Руффини аференти реагују на силе које се нормално примењују на кожу, јединствена карактеристика СА ИИ аферената је њихова способност да реагују и на бочно истезање коже. Коначно, јединице длаке у подлактици имају велика јајолика или неправилна рецептивна поља састављена од више осетљивих тачака које су одговарале појединачним длачицама (свака аферентна опскрба ~20 длака).
Механичка осетљивост кератиноцита
Сваки механички стимуланс на кожи мора се пренети кроз кератиноците који формирају епидермис. Ове свеприсутне ћелије могу обављати сигналне функције поред својих улога подршке или заштите. На пример, кератиноцити луче АТП, важан сензорни сигнални молекул, као одговор на механичке и осмотске стимулусе.54,55 Ослобађање АТП-а индукује повећање интрацелуларног калцијума аутокрином стимулацијом пуринергичких рецептора.55 Надаље, постоје докази да хипотоничност активира Рхо. -киназни сигнални пут и накнадно формирање Ф-актинских стресних влакана што сугерише да механичка деформација кератиноцита може механички ометати суседне ћелије као што су Меркел ћелије за безопасан додир и завршеци слободних Ц-влакна за штетни додир [Сл. 1 (Ц6)].56,57
Нокиоус Тоуцх
Механорецептори високог прага (ХТМР) су епидермални Ц- и А? слободни нервни завршеци. Они нису повезани са специјализованим структурама и примећују се у обе длакаве коже [Сл. 1 (А9)] и гола кожа (Сл. 1(Ц7)]. Међутим, термин слободних нервних завршетака треба узети у обзир опрезно јер су нервни завршеци увек у блиској супротности са кератиноцитним или Лангхерансовим ћелијама или меланоцитима. Ултраструктурна анализа нервних завршетака открива присуство грубог ендоплазматског ретикулума, обилне митохондрије и везикуле густог језгра. Суседне мембране епидермалних ћелија су задебљане и подсећају на постсинаптичку мембрану у нервним ткивима. Имајте на уму да интеракције између нервних завршетака и епидермалних ћелија могу бити двосмерне пошто епидермалне ћелије могу да ослобађају медијаторе као што су АТП, интерлеукин (ИЛ6, ИЛ10) и брадикинин и обрнуто, пептидергични нервни завршеци могу да ослобађају пептиде као што је ЦГРП или супстанца П делујући на ћелије епидерме. ХТМР се састоје од механо-ноцицептора побуђених само штетним механичким стимулусима и полимодалних ноцицептора који такође реагују на штетну топлоту и егзогене хемикалије [Сл. 2 (Б2)].58
ХТМР аферентна влакна завршавају се на пројекционим неуронима у дорзалном рогу кичмене мождине. А?-ХТМР-ови контактирају неуроне другог реда претежно у ламини И и В, док Ц-ХТМР-ови завршавају у ламини ИИ [Сл. 1 (Б8)]. Ноцицептивни неурони другог реда пројектују се на контролну страну кичмене мождине и уздижу се у белу материју, формирајући антеролатерални систем. Ови неурони завршавају углавном у таламусу (Сл. 1 (Б9 и Б10)].
Механо-струје у соматосензорним неуронима
Механизми споре или брзе адаптације механорецептора још нису разјашњени. Није јасно у којој мери прилагођавање механорецептора обезбеђује ћелијско окружење чулних нервних завршетака, интринзична својства механички затворених канала и својства аксоналних напонско-зависних јонских канала у сензорним неуронима (слика 2). Међутим, недавни напредак у карактеризацији механички затворених струја показао је да различите класе механосензитивних канала постоје у ДРГ неуронима и могу објаснити неке аспекте адаптације механорецептора.
Ин витро снимање код глодара показало је да је сома ДРГ неурона интринзично механосензитивна и да изражава катјонске механо-зависне струје.59-64 Гадолинијум и рутенијум црвена у потпуности блокирају механоосетљиве струје, док спољашњи калцијум и магнезијум, у физиолошким концентрацијама, као и амилорид и бензамил, изазивају делимичну блокаду.60,62,63 ФМ1-43 делује као трајни блокатор, а ињекција ФМ1-43 у задњу шапу мишева смањује осетљивост на бол у Рандалл-Селитто тесту и повећава процењени праг повлачења шапе са власи Фон Фреи.65
Као одговор на трајну механичку стимулацију, механоосетљиве струје опадају кроз затварање. На основу временских константи опадања струје, разликују се четири различите врсте механоосетљивих струја: струје које се брзо прилагођавају (~3 мс), средње адаптирајуће струје (~6 мс), споро прилагођавајуће струје (~15 мс ) и струје које се ултра споро прилагођавају (~30 мс).200 Све ове струје су присутне са променљивом инциденцом код ДРГ неурона пацова који инервирају голу кожу задње шапе.300
Механичка осетљивост механосензитивних струја може се одредити применом серије инкременталних механичких стимулуса, омогућавајући релативно детаљну анализу стимулус-струја.66 Однос стимулус–струја је типично сигмоидални, а максимална амплитуда струје је одређена бројем канали који су истовремено отворени.64,67 Занимљиво је да је пријављено да брзо адаптирајућа механоосетљива струја показује низак механички праг и средњу тачку полуактивације у поређењу са ултра-спором адаптирајућом механоосетљивом струјом.63,65
Сензорни неурони са неноцицептивним фенотиповима преференцијално изражавају брзо адаптирајуће механосензитивне струје са нижим механичким прагом.60,61,63,64,68 Насупрот томе, споро и ултра споро прилагођавајуће механосензитивне струје се повремено пријављују у наводним неноцицептивним ћелијама.64,68 Ово је подстакло сугестију да ове струје могу допринети различитим механичким праговима који се виде у ЛТМР и ХТМР ин виво. Иако ове ин витро експерименте треба узети са опрезом, подршку за присуство у соми ДРГ неурона механотрансдуктера ниског и високог прага такође је пружила стимулација култивисаних мишјих сензорних неурона заснована на радијалном истезању.69 Ова парадигма је открила два главне популације неурона осетљивих на истезање, један који реагује на ниску амплитуду стимулуса и други који селективно реагује на високу амплитуду стимулуса.
Ови резултати имају важне, али спекулативне, механичке импликације: механички праг сензорних неурона можда нема много везе са ћелијском организацијом механорецептора, али може лежати у својствима механички затворених јонских канала.
Механизми који леже у основи десензибилизације механоосетљивих катјонских струја у ДРГ неуронима пацова су недавно откривени.64,67 То је резултат два истовремена механизма који утичу на својства канала: адаптација и инактивација. Адаптација је први пут пријављена у студијама слушних ћелија косе. Оперативно се може описати као једноставно превођење криве активације канала трансдуктора дуж осе механичког стимулуса.70-72 Адаптација омогућава сензорним рецепторима да задрже своју осетљивост на нове стимулусе у присуству постојећег стимулуса. Међутим, значајан део механосензитивних струја у ДРГ неуронима не може се поново активирати након условљавања механичке стимулације, што указује на инактивацију неких канала трансдуктора.64,67 Према томе, и инактивација и адаптација делују у тандему да регулишу механосензитивне струје. Ова два механизма су заједничка за све механосензитивне струје идентификоване у ДРГ неуронима пацова, што сугерише да повезани физичко-хемијски елементи одређују кинетику ових канала.64
У закључку, одређивање својстава ендогених механосензитивних струја ин витро је кључно у потрази за идентификацијом механизама трансдукције на молекуларном нивоу. Варијабилност уочена у механичком прагу и кинетици прилагођавања различитих механички управљаних струја у ДРГ неуронима сугеришу да интринзична својства јонских канала могу објаснити, барем делимично, механички праг и кинетику прилагођавања механорецептора описаних у деценијама 1960. 80 користећи ек виво препарате.
Претпостављени механосензитивни протеини
Механосензитивне јонске струје у соматосензорним неуронима су добро окарактерисане, насупрот томе, мало се зна о идентитету молекула који посредују у механотрансдукцији код сисара. Генетски прегледи код Дросопхиле и Ц. елеганс су идентификовали кандидате за молекуле механотрансдукције, укључујући породице ТРП и дегенерин/епителних На+ канала (Дег/ЕНаЦ).73 Недавни покушаји да се разјасни молекуларна основа механотрансдукције код сисара углавном су се фокусирали на ове хомологе кандидата. . Поред тога, многи од ових кандидата су присутни у кожним механорецепторима и соматосензорним неуронима (слика 2).
Јонски канали осетљиви на киселину
АСИЦ-ови припадају протонским подгрупама породице дегенеринских епителних На+ канала.74 Три члана породице АСИЦ (АСИЦ1, АСИЦ2 и АСИЦ3) су изражени у механорецепторима и ноцицепторима. Улога АСИЦ канала је истраживана у студијама понашања на мишевима са циљаним брисањем гена АСИЦ канала. Брисање АСИЦ1 не мења функцију кожних механорецептора, али повећава механичку осетљивост аферената који инервирају црева.75 АСИЦ2 нокаут мишеви показују смањену осетљивост брзо прилагођавајућих кожних ЛТМР-а.76 Међутим, касније студије су пријавиле недостатак ефеката нокаутирања АСИЦ2 на и висцерална механо-ноцицепција и кожна механосензација.77 АСИЦ3 поремећај смањује механо осетљивост висцералних аферената и смањује одговоре кожних ХТМР-ова на штетне стимулусе.76
Транзијентни рецепторски канал
ТРП суперфамилија је подељена на шест подфамилија код сисара.78 Скоро све ТРП подфамилије имају чланове повезане са механосензијом у различитим ћелијским системима.79 У сензорним неуронима сисара, међутим, ТРП канали су најпознатији по детекцији термалних информација и посредовању неурогене упале, а само два ТРП канала, ТРПВ4 и ТРПА1, су укључена у одзив на додир. Поремећај експресије ТРПВ4 код мишева има само скромне ефекте на акутне механосензорне прагове, али снажно смањује осетљивост на штетне механичке стимулусе.80,81 ТРПВ4 је кључна детерминанта у обликовању одговора ноцицептивних неурона на осмотски стрес и механичку хипералгезију.82,83 током инфламације,1мммм. 1 Чини се да ТРПА1 има улогу у механичкој хипералгезији. Мишеви са недостатком ТРПА84,85 показују преосетљивост на бол. ТРПАXNUMX доприноси трансдукцији механичких, хладних и хемијских стимулуса у сензорним неуронима ноцицептора, али изгледа да то није од суштинског значаја за трансдукцију ћелија косе.XNUMX
Нема јасних доказа који указују на то да су ТРП канали и АСИЦ канали изражени код сисара механички затворени. Ниједан од ових канала изражених хетерологно не рекапитулира електрични потпис механоосетљивих струја уочених у њиховом природном окружењу. Ово не искључује могућност да су АСИЦ и ТРП канали механотрансдуктори, с обзиром на неизвесност да ли канал механотрансдукције може да функционише ван свог ћелијског контекста (погледајте одељак о СЛП3).
Пиезо протеини
Пиезо протеини су недавно идентификовани као обећавајући кандидати за механосенсинг протеине од стране Коста и сарадника.86,87 Кичмењаци имају два Пиезо члана, Пиезо 1 и Пиезо 2, раније познати као ФАМ38А и ФАМ38Б, респективно, који су добро очувани у вишећелијском еуку. . Пиезо 2 има у изобиљу ДРГ, док се Пиезо 1 једва може детектовати. Пиезо-индуковане механосензитивне струје спречавају инхибирање гадолинијумом, рутенијум црвеним и ГсМТк4 (токсином из тарантуле Граммостола спатулата).88 Експресија Пиезо 1 или Пиезо 2 у хетерологним системима производи механоосетљиве струје, при чему је кинетика Пиезоацтив струје брзе струје2. него Пиезо 1. Слично ендогеним механосензитивним струјама, Пиезо зависне струје имају реверзибилне потенцијале око 0 мВ и нису селективне за катјоне, при чему На+, К+, Ца2+ и Мг2+ сви прожимају канал испод. Слично, пиезо зависне струје су регулисане мембранским потенцијалом, уз значајно успоравање кинетике струје при деполаризованим потенцијалима.86
Пиезо протеини су несумњиво протеини за механосензивање и деле многа својства брзо прилагођавајућих механосензитивних струја у сензорним неуронима. Третман култивисаних ДРГ неурона са Пиезо 2 кратком интерферирајућом РНК смањио је удео неурона са струјом која се брзо прилагођава и смањио проценат механосензитивних неурона.86 Трансмембрански домени се налазе у целом пиезо протеинима, али нису откривени очигледни мотиви који садрже поре или потписи јонских канала. идентификован. Међутим, мишји Пиезо 1 протеин пречишћен и реконституисан у асиметричне липидне двослојеве и липозом формира јонске канале осетљиве на рутенијум црвено.87 Суштински корак у валидацији механотрансдукције кроз Пиезо канале је коришћење ин виво приступа за одређивање функционалног значаја у сигнализацији додира. Информације су дате у Дросопхили где је брисање једног члана Пиезо смањило механички одговор на штетне стимулусе, без утицаја на нормалан додир.89 Иако њихова структура остаје да се утврди, ова нова породица механосензитивних протеина је обећавајући предмет за будућа истраживања, изван граница осећаја додира. На пример, недавна студија на пацијентима са анемијом (наследна ксероцитоза) показује улогу Пиезо 1 у одржавању хомеостазе запремине еритроцита.90
Слично трансмембранском каналу (ТМЦ)
Недавна студија указује да су два протеина, ТМЦ1 и ТМЦ2, неопходна за механотрансдукцију ћелија длаке.91 Наследна глувоћа услед мутације ТМЦ1 гена је пријављена код људи и мишева.92,93 Присуство ових канала још увек није показано у соматосензорном систему. , али изгледа да је то добар повод за истраживање.
Протеин сличан стоматину 3 (СЛП3)
Поред трансдукционих канала, показало се да неки помоћни протеини повезани са каналом играју улогу у осетљивости на додир. СЛП3 је експримиран у ДРГ неуронима сисара. Студије које су користиле мутантне мишеве којима недостаје СЛП3 су показале промену у механосензицији и механосензивним струјама.94,95 Прецизна функција СЛП3 остаје непозната. То може бити линкер између механосензитивног канала и микротубула који леже у позадини, као што је предложено за његов хомолог Ц. елеганс МЕЦ2.96 Недавно ГР. Лабораторија Левин је сугерисала да се привез синтетишу ДРГ сензорни неурони и да повезује механоосетљиви јонски канал са екстрацелуларним матриксом.97 Прекид везе укида струју РА-механосензитивну, што сугерише да су неки јонски канали механоосетљиви само када су везани. РА-механосензитивне струје су такође инхибиране ламинином-332, матриксним протеином који производе кератиноцити, појачавајући хипотезу о модулацији механоосетљиве струје екстрацелуларним протеинима.98
Подфамилија канала К+
Паралелно са катјонским деполаризујућим механоосетљивим струјама, истражује се присуство реполаризујућих механоосетљивих К+ струја. К+ канали у механосензитивним ћелијама могу ући у тренутни баланс и допринети дефинисању механичког прага и временског тока адаптације механорецептора.
Чланови КЦНК припадају породици К+ канала са доменом са две поре (К2П).99,100 К2П показује изузетан опсег регулације путем ћелијских, физичких и фармаколошких агенаса, укључујући пХ промене, топлоту, истезање и деформацију мембране. Ови К2П су активни у мембранском потенцијалу мировања. Неколико КЦНК подјединица је експримирано у соматосензорним неуронима.101 Канали КЦНК2 (ТРЕК-1), КЦНК4 (ТРААК) и ТРЕК-2 су међу ријетким каналима за које је приказано директно механичко гајтирање растезањем мембране.102,103
Мишеви са поремећеним КЦНК2 геном показали су повећану осетљивост на топлоту и благе механичке стимулусе, али нормалан праг повлачења штетног механичког притиска примењеног на задњу шапу коришћењем Рандалл-Селитто теста.104 Мишеви са недостатком КЦНК2 такође показују повећану термичку и механичку хипералгезију код инфламаторних Услови. КЦНК4 нокаут мишеви су били преосетљиви на благу механичку стимулацију, а ова преосетљивост је повећана додатном инактивацијом КЦНК2.105 Повећана механосензитивност ових нокаут мишева могла би значити да истезање нормално активира и деполаризирајуће и реполаризирајуће механосензитивне струје, на сличан начин на неусклађени начин. деполаризујућих и реполаризујућих напонских струја.
КЦНК18 (ТРЕСК) је главни фактор који доприноси позадинској К+ проводљивости која регулише потенцијал мембране у мировању соматосензорних неурона.106 Иако није познато да ли је КЦНК18 директно осетљив на механичку стимулацију, може играти улогу у посредовању одговора на лагани додир, као и болни механички надражаји. КЦНК18 и у мањој мери КЦНК3, су предложени као молекуларна мета хидрокси-а-сансхоол-а, једињења пронађеног у зрну бибера Шезуан које активира рецепторе додира и изазива осећај пецкања код људи.107,108
К+ канал зависан од напона КЦНК4 (Кв7.4) је кључан за подешавање брзине и преференције фреквенције субпопулације механорецептора који се брзо прилагођава и код мишева и код људи. Мутација КЦНК4 је у почетку била повезана са обликом наследне глувоће. Занимљиво је да је недавна студија локализовала КЦНК4 у периферним нервним завршецима кожног фоликула длаке који се брзо прилагођава и Меисснеровог тела. Сходно томе, губитак КЦНК4 функције доводи до селективног побољшања осетљивости механорецептора на нискофреквентне вибрације. Посебно, људи са касним губитком слуха због доминантних мутација гена КЦНК4 показују побољшане перформансе у откривању вибрација мале амплитуде, ниске фреквенције.109

Увид др Алек Јименез-а
Додир се сматра једним од најсложенијих чула у људском телу, посебно зато што за то не постоји посебан орган задужен. Уместо тога, чуло додира се јавља преко сензорних рецептора, познатих као механорецептори, који се налазе преко коже и реагују на механички притисак или изобличење. Постоје четири главна типа механорецептора у голој, или без длаке, кожи сисара: ламеларно тело, тактилно тело, Меркелове нервне завршетке и луковичасто тело. Механорецептори функционишу како би омогућили детекцију додира, како би пратили положај мишића, костију и зглобова, познат као проприоцепција, па чак и да би детектовали звукове и кретање тела. Разумевање механизама структуре и функције ових механорецептора је основни елемент у коришћењу третмана и терапија за управљање болом.
Zakljucak
Додир је комплексно чуло јер представља различите тактилне квалитете, односно вибрацију, облик, текстуру, задовољство и бол, са различитим дискриминативним перформансама. До сада је подударност између органа додира и психофизичког чула била корелативна и тек се појављују класно-специфични молекуларни маркери. Сада је неопходан развој тестова за глодаре који одговарају разноликости понашања на додир како би се олакшала будућа геномичка идентификација. Употреба мишева који немају специфичне подскупове сензорних аферентних типова ће у великој мери олакшати идентификацију механорецептора и сензорних аферентних влакана повезаних са одређеним модалитетом додира. Занимљиво је да недавни рад отвара важно питање генетске основе механосензорних особина код људи и сугерише да би мутација једног гена могла негативно утицати на осетљивост на додир.110 Ово подвлачи да је патофизиологија дефицита додира код људи у великој мери непозната и да би сигурно напредују тако што прецизно идентификују подскуп сензорних неурона повезаних са модалитетом додира или дефицитом додира.
Заузврат, постигнут је напредак у дефинисању биофизичких својстава механизованих струја.64 Развој нових техника последњих година, који омогућавају праћење промена напетости мембране, уз снимање механизоване струје, показао се вредним експерименталним методом за описивање механосензитивне струје са брзом, средњем и спором адаптацијом (прегледано у Делмасу и сарадницима).66,111 Будућност ће бити утврђивање улоге својстава струје у механизмима адаптације функционално различитих механорецептора и доприноса механосензитивних К+ струја ексцитабилности ЛТМР и ХТМР.
Молекуларна природа механизованих струја код сисара је такође тема истраживања која обећавају. Будућа истраживања ће напредовати у две перспективе, прво да би се утврдила улога помоћног молекула који везује канале за цитоскелет и који би био потребан да додели или регулише механосензитивност јонских канала попут ТРП и АСИЦ/ЕнаЦ породица. Друго, истражити велику и обећавајућу област доприноса Пиезо канала тако што ћемо одговорити на кључна питања, у вези са механизмима прожимања и затварања, подскуп сензорних неурона и модалитета додира који укључује Пиезо и улогу Пиезо у не-неуронским ћелијама повезаним са механосензација.
Чуло додира, у поређењу са оним вида, укуса, звука и мириса, који користе специфичне органе за обраду ових сензација, може се јавити у целом телу преко сићушних рецептора познатих као механорецептори. Различити типови механорецептора се могу наћи у различитим слојевима коже, где могу открити широк спектар механичких стимулација. Чланак изнад описује специфичне нагласке који показују напредак структурних и функционалних механизама механорецептора повезаних са чулом додира. Информације пренете из Националног центра за биотехнолошке информације (НЦБИ). Обим наших информација је ограничен на киропрактику, као и на повреде и стања кичме. Да бисте разговарали о овој теми, слободно питајте др Хименеза или нас контактирајте на�915-850-0900 .
Курирао др Алек Јименез
Додатне теме: Бол у леђима
Бол у леђима је један од најчешћих узрока инвалидности и пропуштених дана на послу широм света. Заправо, болови у леђима приписани су као други најчешћи разлог посета лекарској ординацији, надмашени само инфекцијама горњих дисајних путева. Отприлике 80 процената становништва ће се барем једном током живота суочити са неком врстом болова у леђима. Кичма је сложена структура коју између осталих меких ткива чине кости, зглобови, лигаменти и мишићи. Због тога су повреде и / или отежани услови, као нпр хернија дискова, на крају може довести до симптома болова у леђима. Спортске повреде или повреде у аутомобилским несрећама често су најчешћи узрок болова у леђима, али понекад најједноставнији покрети могу имати болне резултате. Срећом, алтернативне опције лечења, попут хиропрактичке неге, могу помоћи у ублажавању болова у леђима употребом кичмених подешавања и ручних манипулација, на крају побољшавајући ублажавање болова.

ДОДАТНА ВАЖНА ТЕМА: Управљање боловима у леђима
ЈОШ ТЕМА: ДОДАТНО: Хронични бол и третмани
Бланк
Референце
Затвори Хармоника
Информације овде о „Структурни и функционални механизми механорецептора" није намењен да замени однос један на један са квалификованим здравственим радником или лиценцираним лекаром и није медицински савет. Подстичемо вас да доносите одлуке о здравственој заштити на основу вашег истраживања и партнерства са квалификованим здравственим радником.
Информације о блогу и дискусије о обиму
Наш обим информација је ограничен на киропрактику, мускулоскелетну, физикалне лекове, веллнесс, доприносећи етиолошкој висцеросоматски поремећаји унутар клиничких презентација, повезане клиничке динамике соматовисцералног рефлекса, комплекса сублуксације, осетљивих здравствених проблема и/или чланака, тема и дискусија функционалне медицине.
Пружамо и представљамо клиничка сарадња са специјалистима из разних дисциплина. Сваки специјалиста се руководи својим професионалним обимом праксе и јурисдикцијом лиценцирања. Користимо функционалне здравствене и веллнесс протоколе за лечење и подршку нези повреда или поремећаја мишићно-скелетног система.
Наши видео снимци, постови, теме, теме и увиди покривају клиничка питања, проблеме и теме које се односе на и директно или индиректно подржавају наш клинички обим праксе.*
Наша канцеларија је разумно покушала да обезбеди цитате у прилог и идентификовала је релевантну истраживачку студију или студије које подржавају наше објаве. На захтев пружамо копије пратећих истраживачких студија доступне регулаторним одборима и јавности.
Разумемо да покривамо питања која захтевају додатно објашњење како то може помоћи у одређеном плану неге или протоколу лечења; зато, да бисте даље разговарали о горњој теми, слободно питајте Др Алек Јименез, ДЦ, или нас контактирајте 915-850-0900.
Овде смо да помогнемо вама и вашој породици.
Благослови
Др. Алек Јименез ДЦ, МСАЦП, РН*, ЦЦСТ, ИФМЦП*, ЦИФМ*, АТН*
e-маил: цоацх@елпасофунцтионалмедицине.цом
Лиценцирани као доктор киропрактике (ДЦ) у Тексас & Нови Мексико*
Тексас ДЦ лиценца бр. ТКСКСНУМКС, Нев Мекицо ДЦ Лиценца # НМ-ДЦ2182
Лиценцирана као медицинска сестра (РН*) in Флорида
Флорида лиценца РН лиценца # РНКСНУМКС (Контролни бр. 3558029)
Компактни статус: Вишедржавна лиценца: Овлашћени за праксу у КСНУМКС државе*
Др Алек Јименез ДЦ, МСАЦП, РН* ЦИФМ*, ИФМЦП*, АТН*, ЦЦСТ
Моја дигитална визит карта







